题目内容
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如图1所示(KMnO4溶液已酸化):
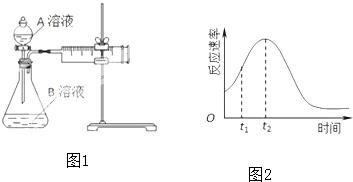
(1)该实验探究的是 因素对化学反应速率的影响.相同时间内针筒中所得CO2的体积大小关系是① ②(填“>”、“<”或“=”).
(2)若实验①在2min末收集了4.48mL CO2(标准状况下),则在2min末,c(MnO4-)= mol?L-1.(假设混合溶液体积为50mL)
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率.
(4)小组同学发现反应速率总是如图2,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂、② .

| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol?L-1H2C2O4溶液 | 30mL 0.01mol?L-1KMnO4溶液 |
| ② | 20mL 0.2mol?L-1H2C2O4溶液 | 30mL 0.01mol?L-1KMnO4溶液 |
(2)若实验①在2min末收集了4.48mL CO2(标准状况下),则在2min末,c(MnO4-)=
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定
(4)小组同学发现反应速率总是如图2,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂、②
考点:探究影响化学反应速率的因素
专题:实验设计题
分析:(1)对比①②实验可探究浓度对化学反应速率的影响,②中A溶液的浓度比①中大;
(2)先求出反应的(MnO4-)的物质的量,再求出反应后的浓度;
(3)通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率;
(4)从影响化学反应速率的因素主要有温度、浓度、压强和催化剂考虑.
(2)先求出反应的(MnO4-)的物质的量,再求出反应后的浓度;
(3)通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率;
(4)从影响化学反应速率的因素主要有温度、浓度、压强和催化剂考虑.
解答:
解:(1)对比①②实验可探究浓度对化学反应速率的影响,②中A溶液的浓度比①中大,化学反应速率大,所得CO2的体积大,故答案为:浓度;<;
(2)CO2的物质的量是:4.48mL×10-322.4mol/l=0.0002mol,设2min末,反应(MnO4-)为X,
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
2 10
X 0.0002mol
解得 X=0.00004mol
30mL×10-3×0.01mol?L-1-0.00004mol=0.00026mol
C(MnO4-)=nv=0.00026mol0.05L=0.0052mol/L
故答案为:0.0052;
(3)通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率,
故答案为:KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间;
(4)影响化学反应速率的因素主要有温度、浓度、压强和催化剂,除催化剂之外,只能是温度升高导致反应速率加快,故答案为:该反应放热使反应温度升高.
(2)CO2的物质的量是:4.48mL×10-322.4mol/l=0.0002mol,设2min末,反应(MnO4-)为X,
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
2 10
X 0.0002mol
解得 X=0.00004mol
30mL×10-3×0.01mol?L-1-0.00004mol=0.00026mol
C(MnO4-)=nv=0.00026mol0.05L=0.0052mol/L
故答案为:0.0052;
(3)通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率,
故答案为:KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间;
(4)影响化学反应速率的因素主要有温度、浓度、压强和催化剂,除催化剂之外,只能是温度升高导致反应速率加快,故答案为:该反应放热使反应温度升高.
点评:本题考查了影响化学反应速率的因素,难度不大,注意可通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
将甘油溶解于甲苯中得到一混合物,若其中碳元素的质量分数为50%,那么氧元素的质量分数为( )
| A、41.3% | B、8.7% |
| C、1.74% | D、无法计算 |
氧化还原反应的实质是( )
| A、得到氧元素与失去氧元素 |
| B、有无新物质生成 |
| C、化合价的升降 |
| D、电子的得失或共用电子对的偏移 |
某课外小组做了一个有趣的实验,将2g铝粉和3g碘粉小心混合均匀,分成相等三份,分别进行实验,现将实验记录列表:
根据上述实验事实,作出的推断错误的是( )
| 第一组 | 加入0.5g水 | 很快产生火花 |
| 第二组 | 加入1g胆矾 | 约30s产生火花 |
| 第三组 | 加入1g无水硫酸铜 | 1min内没有明显现象 |
| A、水能加快铝和碘的反应 |
| B、第三组铝和硫酸铜发生了置换反应 |
| C、第一组和第二组实验中均放出热量 |
| D、第一组实验中铝和碘发生反应生成了AlI3 |
下列说法正确的是( )
A、按系统命名法,化合物  的名称是2,3,5,5-四甲-4,4-二乙基己烷 的名称是2,3,5,5-四甲-4,4-二乙基己烷 |
| B、等质量的乙烯和2-甲基-2-丁烯完全燃烧消耗氧气的量不相等 |
| C、分子式为C10H20的烯烃分子中的10个C原子可能在一个平面上 |
| D、分子式为C8H18的分子中的所有C原子不可能都在一个平面上 |
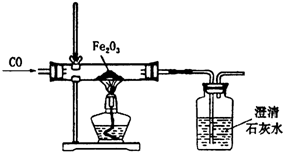 某课外活动小组在实验室条件下探究CO与Fe2O3反应的产物情况,实验设计如图所示.
某课外活动小组在实验室条件下探究CO与Fe2O3反应的产物情况,实验设计如图所示.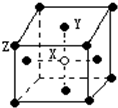 (1)某晶体的晶胞如图所示,X位于体心,Y位于6面心,Z位于顶点,该晶体中 X、Y、Z的粒子个数比为
(1)某晶体的晶胞如图所示,X位于体心,Y位于6面心,Z位于顶点,该晶体中 X、Y、Z的粒子个数比为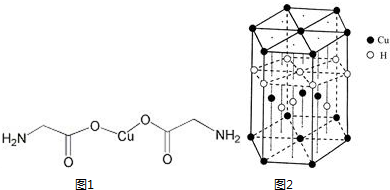 锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3?H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3?H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O