题目内容
中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g?L-1.某兴趣小组用如图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定.
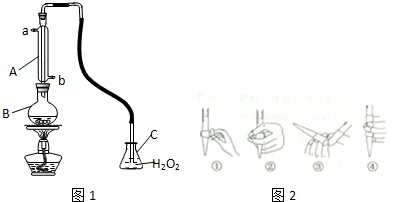
(1)仪器A的名称是 ,水通入A的进口为 .
(2)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为 .
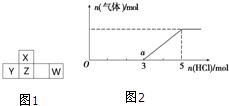
(3)除去C中过量的H2O2,然后用0.0900mol?L-1 NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的 ;若滴定终点时溶液的pH=8.8,则选择的指示剂为 ;若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积 (填序号)(①=10mL,②=40mL,③<10mL,④>40mL)
(4)滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为 g?L-1
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施: .

(1)仪器A的名称是
(2)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为
(3)除去C中过量的H2O2,然后用0.0900mol?L-1 NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的
(4)滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施:
考点:真题集萃,二氧化硫的化学性质,探究物质的组成或测量物质的含量
专题:氧族元素
分析:(1)根据仪器A特点书写其名称,为了充分冷却气体,应该下口进水;
(2)二氧化硫具有还原性,能够与实验室反应生成硫酸,据此写出反应的化学方程式;
(3)氢氧化钠应该盛放在碱式滴定管中,根据碱式滴定管的排气泡法进行判断;根据滴定终点时溶液的pH及常见指示剂的变色范围选用正确的指示剂;根据滴定管的构造判断滴定管中溶液的体积;
(4)根据关系式2NaOH~H2SO4~SO2及氢氧化钠的物质的量计算出二氧化硫的质量,再计算出该葡萄酒中的二氧化硫含量;
(5)根据盐酸是挥发性酸,挥发的酸消耗氢氧化钠判断对测定结果的影响;可以选用非挥发性的酸或用蒸馏水代替葡萄酒进行对比实验,减去盐酸挥发的影响.
(2)二氧化硫具有还原性,能够与实验室反应生成硫酸,据此写出反应的化学方程式;
(3)氢氧化钠应该盛放在碱式滴定管中,根据碱式滴定管的排气泡法进行判断;根据滴定终点时溶液的pH及常见指示剂的变色范围选用正确的指示剂;根据滴定管的构造判断滴定管中溶液的体积;
(4)根据关系式2NaOH~H2SO4~SO2及氢氧化钠的物质的量计算出二氧化硫的质量,再计算出该葡萄酒中的二氧化硫含量;
(5)根据盐酸是挥发性酸,挥发的酸消耗氢氧化钠判断对测定结果的影响;可以选用非挥发性的酸或用蒸馏水代替葡萄酒进行对比实验,减去盐酸挥发的影响.
解答:
解:(1)根据仪器A的构造可知,仪器A为冷凝管,冷凝管中通水方向采用逆向通水法,冷凝效果最佳,所以应该进水口为b,
故答案为:冷凝管或冷凝器;b;
(2)双氧水具有氧化性,能够将二氧化硫氧化成硫酸,反应的化学方程式为:SO2+H2O2=H2SO4,
故答案为:SO2+H2O2=H2SO4;
(3)氢氧化钠溶液为碱性溶液,应该使用碱式滴定管,碱式滴定管中排气泡的方法:把滴定管的胶头部分稍微向上弯曲,再排气泡,所以排除碱式滴定管中的空气用③的方法;滴定终点时溶液的pH=8.8,应该选择酚酞做指示剂(酚酞的变色范围是8.2~10.0);若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,滴定管的0刻度在上方,10mL刻度线下方还有40mL有刻度的溶液,另外滴定管50mL刻度线下有液体,因此管内的液体体积>(50.00mL-10.00mL)=40.00mL,所以④正确,
故答案为:③;酚酞;④;
(4)根据2NaOH~H2SO4~SO2可知SO2的质量为:
×(0.0900mol/L×0.025L)×64g/mol=0.072g,该葡萄酒中的二氧化硫含量为:
=0.24g/L,
故答案为:0.24;
(5)由于盐酸是挥发性酸,挥发的酸消耗氢氧化钠,使得消耗的氢氧化钠溶液体积增大,测定结果偏高;因此改进的措施为:用不挥发的强酸,如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响,
故答案为:原因:盐酸的挥发;改进措施:用不挥发的强酸如硫酸代替盐酸(或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响).
故答案为:冷凝管或冷凝器;b;
(2)双氧水具有氧化性,能够将二氧化硫氧化成硫酸,反应的化学方程式为:SO2+H2O2=H2SO4,
故答案为:SO2+H2O2=H2SO4;
(3)氢氧化钠溶液为碱性溶液,应该使用碱式滴定管,碱式滴定管中排气泡的方法:把滴定管的胶头部分稍微向上弯曲,再排气泡,所以排除碱式滴定管中的空气用③的方法;滴定终点时溶液的pH=8.8,应该选择酚酞做指示剂(酚酞的变色范围是8.2~10.0);若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,滴定管的0刻度在上方,10mL刻度线下方还有40mL有刻度的溶液,另外滴定管50mL刻度线下有液体,因此管内的液体体积>(50.00mL-10.00mL)=40.00mL,所以④正确,
故答案为:③;酚酞;④;
(4)根据2NaOH~H2SO4~SO2可知SO2的质量为:
| 1 |
| 2 |
| 0.72g |
| 0.3L |
故答案为:0.24;
(5)由于盐酸是挥发性酸,挥发的酸消耗氢氧化钠,使得消耗的氢氧化钠溶液体积增大,测定结果偏高;因此改进的措施为:用不挥发的强酸,如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响,
故答案为:原因:盐酸的挥发;改进措施:用不挥发的强酸如硫酸代替盐酸(或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响).
点评:本题为一道高考题,考查了探究物质的组成、测量物质的含量的方法,题目难度中等,试题涉及了二氧化硫性质、中和滴定的计算,要求学生掌握探究物质组成、测量物质含量的方法,明确二氧化硫的化学性质及中和滴定的操作方法及计算方法,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
以氧化铝为原料制取氢氧化铝,最好的方法是( )
| A、将氧化铝溶于水 |
| B、将氧化铝先溶于盐酸中,之后滴加氨水 |
| C、将氧化铝溶于盐酸中,之后滴加氢氧化钠溶液 |
| D、将氧化铝溶于氢氧化钾 |
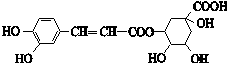 下列有关绿原酸(结构简式如图)的说法不正确的是( )
下列有关绿原酸(结构简式如图)的说法不正确的是( )| A、分子式为C16H18O9 |
| B、1mol绿原酸最多能与8mol NaOH反应 |
| C、1mol绿原酸最多能与4mol H2反应 |
| D、能发生取代反应、消去反应、加成反应和氧化反应 |
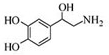 去甲肾上腺素可以调控动物机体的植物性神经功能,其结构简式如图所示,下列说法正确的是( )
去甲肾上腺素可以调控动物机体的植物性神经功能,其结构简式如图所示,下列说法正确的是( )| A、每个去甲肾上腺素分子中含有3个酚羟基 |
| B、每个去甲肾上腺素分子中含有1个手性碳原子 |
| C、1mol去甲肾上腺素最多与2mol Br2发生取代反应 |
| D、去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |


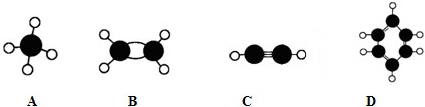
 短周期元素X、Y、Z、W在周期表中的位置如图1所示,其中W的氧化物是酸雨形成的主要物质.
短周期元素X、Y、Z、W在周期表中的位置如图1所示,其中W的氧化物是酸雨形成的主要物质.
