题目内容
12.下列各组物质中,物质之间通过一步反应就能实现图示变化的是( )| 物质编号 | 物质转化关系 | a | b | c | d |
| A | 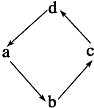 | N2 | NO2 | NO | HNO3 |
| B | Na | Na2O2 | NaOH | NaCl | |
| C | Si | SiO2 | H2SiO3 | Na2SiO3 | |
| D | Al2O3 | NaAlO2 | Al | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.氮气不能一步转化为NO2;
B.钠与氧气反应生成Na2O2,Na2O2与水反应生成NaOH,NaOH与盐酸反应生成NaCl,电解NaCl生成Na;
C.SiO2不能一步转化为H2SiO3;
D.NaAlO2不能一步转化为Al,Al不能一步转化为Al(OH)3.
解答 解:A.氮气只能一步转化为NO,氮气不能一步转化为NO2,不符合图中转化,故A错误;
B.Na$\stackrel{O_{2}}{→}$Na2O2$\stackrel{H_{2}O}{→}$NaOH$\stackrel{HCl}{→}$NaCl$\stackrel{电解}{→}$Na,均可一步转化,符合图中转化,故B正确;
C.SiO2不能一步转化为H2SiO3,不符合图中转化,故C错误;
D.NaAlO2不能一步转化为Al,Al不能一步转化为Al(OH)3,不符合图中转化,故D错误;
故选B.
点评 本题考查常见金属及化合物的性质,为高频考点,把握物质的性质、发生的反应等为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
3.20mL0.02mol•L-1 KMnO4溶液恰好与20mL0.05mol•L-1 Na2SO3溶液完全反应,则Mn在还原产物中的化合价是:(提示:Na2SO3在反应中被氧化成Na2SO4)( )
| A. | 0 | B. | +2 | C. | +3 | D. | +6 |
20.有关下列四个常用电化学装置的叙述中,正确的是( )
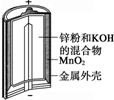 | 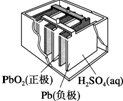 | 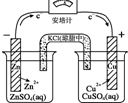 | 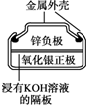 |
| Ⅰ.碱性锌锰电池 | Ⅱ.铅-硫酸蓄电池 | Ⅲ.铜锌原电池 | Ⅳ.银锌纽扣电池 |
| A. | Ⅰ所示电池工作中,MnO2的作用是催化剂 | |
| B. | Ⅱ所示电池放电过程中,硫酸浓度不断增大 | |
| C. | Ⅲ所示电池工作过程中,盐桥中K+移向硫酸锌溶液 | |
| D. | Ⅳ所示电池放电过程中,Ag2O是氧化剂,电池工作过程中还原为Ag |
7.常温下用惰性电极电解NaHSO4溶液,电解一段时间后,下列有关电解质溶液变化的说法正确的是( )
| A. | 电解质溶液的浓度增大,pH减小 | B. | 电解质溶液的浓度增大,pH增大 | ||
| C. | 电解质溶液的浓度减小,pH减小 | D. | 电解质溶液的浓度不变,pH不变 |
17.下表是部分短周期元素在周期表中的相对位置关系,试完成以下题目:
(1)表中元素⑤的氯化物的化学式为NCl3,此氯化物的水溶液显酸性.
(2)写出元素⑦在周期表中的位置为第三周期第ⅡA族.
(3)写出元素⑧的单质与NaOH溶液反应的化学方程式2Al+2H2O+2NaOH═2NaAlO2+3H2↑.
(4)某元素的单质在与大气的平流层中能吸收紫外线,被称为地球生物的“保护伞”,则该元素在表中的序号为⑤,该元素的名称为臭氧
(5)元素⑩的单质是一种污染大气的气体,试写出在实验室中吸收该气体的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
| 族 短周期 | ⅠA | ||||||
| ① | |||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||
| ⑦ | ⑧ | ⑨ | ⑩ |
(2)写出元素⑦在周期表中的位置为第三周期第ⅡA族.
(3)写出元素⑧的单质与NaOH溶液反应的化学方程式2Al+2H2O+2NaOH═2NaAlO2+3H2↑.
(4)某元素的单质在与大气的平流层中能吸收紫外线,被称为地球生物的“保护伞”,则该元素在表中的序号为⑤,该元素的名称为臭氧
(5)元素⑩的单质是一种污染大气的气体,试写出在实验室中吸收该气体的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
3.下列说法正确的是( )
| A. | 原子序数越大,原子半径一定越大 | |
| B. | 电子层数多的原子半径一定比电子层数少的原子半径大 | |
| C. | 元素性质的周期性变化不是元素性质的简单重复 | |
| D. | 按C、N、O、F的顺序,元素的最高正价依次升高 |
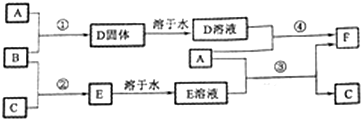
 2SO4(s) D.CH3COONa溶液
2SO4(s) D.CH3COONa溶液