题目内容
下列除杂质的方法中正确的是( )
| A、乙醇中混有乙酸,加入NaOH溶液后,用分液漏斗分液 |
| B、乙烷中混有乙烯,通入H2,在一定条件下反应使乙烯完全转化成乙烷 |
| C、苯甲醛中混有苯甲酸,加入生石灰后,再加热蒸馏 |
| D、溴苯中含有单质溴加入KI溶液后用分液漏斗分液 |
考点:物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作
分析:A.乙醇和水混溶;
B.不能确定乙烯的含量,易混入新杂质;
C.苯甲酸可与生石灰反应;
D.生成的碘易溶于溴苯.
B.不能确定乙烯的含量,易混入新杂质;
C.苯甲酸可与生石灰反应;
D.生成的碘易溶于溴苯.
解答:
解:A.乙醇和水混溶,应用蒸馏的方法除杂,故A错误;
B.不能确定乙烯的含量,易混入新杂质,且在实验室难以完成,故B错误;
C.苯甲酸可与生石灰反应,生成的盐不挥发,可用蒸馏的方法分离,故C正确;
D.生成的碘易溶于溴苯,应加入氢氧化钠溶液除杂,故D错误.
故选C.
B.不能确定乙烯的含量,易混入新杂质,且在实验室难以完成,故B错误;
C.苯甲酸可与生石灰反应,生成的盐不挥发,可用蒸馏的方法分离,故C正确;
D.生成的碘易溶于溴苯,应加入氢氧化钠溶液除杂,故D错误.
故选C.
点评:本题考查混合物的分离、提纯,为高频考点,侧重物质的性质及除杂的考查,把握物质性质的差异及除杂的方法、原则为解答的关键,注意除杂时不能引入新杂质,更不能影响被提纯物质的性质.

练习册系列答案
相关题目
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断错误的是( )
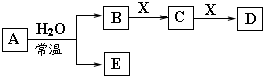

| A、若D为CO,C能和E反应,则A一定不是单质 |
| B、若X是Na2CO3,C为CO2,则A一定是氯气,且D和E不反应 |
| C、若A是单质,B和D的反应是OH-+HCO3-=CO32-+H2O,则E是一种清洁的能源 |
| D、若C的相对分子质量比D小16,B可以使紫色石蕊试液变色,则D一定能与冷水反应 |
下列属于含共价键的分子晶体的是( )
| A、干冰 | B、二氧化硅 |
| C、固态氩 | D、NaOH晶体 |
火法炼铜过程中发生如下反应:Cu2S+O2═2Cu+SO2.下列说法正确的是( )
| A、Cu2S是还原剂,O2是氧化剂 |
| B、Cu是还原产物,SO2是氧化产物 |
| C、1 mol Cu2S和O2反应生成2 mol Cu,转移电子数的物质的量为6 mol |
| D、反应消耗3 mol Cu2S时,被O2氧化的硫(S)的物质的量为3 mol |
下表是几种物质在指定温度下的溶解度(g).现将相同物质的量的NaCl、CO2、NH3在30℃时制成溶液,此时溶液中无晶体,当降温至某温度时,开始析出晶体,此晶体是( )
| 温度 | 0℃ | 10℃ | 20℃ | 30℃ |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.1 |
| NH4HCO3 | 11.9 | 15.9 | 21.0 | 27.0 |
| NaHCO3 | 6.9 | 8.15 | 9.6 | 11.1 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 |
| A、NH4Cl |
| B、NH4HCO3 |
| C、NaHCO3 |
| D、NaCl |
下列对铯及其化合物的预测正确的是( )
| A、铯的熔点很高 |
| B、在自然界中,铯能以游离态存在 |
| C、氯化铯易溶于水 |
| D、铯只有一种氧化物Cs2O |
根据相应的图象(图象编号与答案对应),判断下列相关说法正确的是( )
A、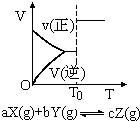 密闭容器中反应达到平衡,t0时改变某一条件有如图变化所示,则改变的条件一定是加入催化剂 |
B、 反应达到平衡时,外界条件对平衡影响关系如图所示,则正反应为放热反应, 且a>b |
C、 物质的百分含量和温度关系如图所示,则该反应的正反应为吸热反应 |
D、 反应速率和反应条件变化关系如图所示,则该反应的正反应为放热反应,A、B、C是气体、D为固体或液体 |
关于化学反应与能量的说法正确的是( )
| A、燃烧属于放热反应 |
| B、反应物总能量与生成物总能量一定相等 |
| C、形成化学键时吸收能量 |
| D、中和反应是吸热反应 |
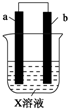 下列对如图所示装置实验判断的描述正确的是( )
下列对如图所示装置实验判断的描述正确的是( )