题目内容
在一恒容密闭容器中充满NO2,常温下建立下列平衡:2NO2(g)?N2O4(g)△H<0,将容器置于100℃的水浴中,则下列性质不改变的是( )
| A、颜色 | B、压强 |
| C、质量 | D、平均相对分子质量 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:可逆反应2NO2?N2O4,正反应放热,升高温度,化学平衡向着吸热方向进行,所以化学平衡2NO2?N2O4向左进行,
A、二氧化氮的浓度增大,颜色加深;
B、升高温度,化学平衡向左移动,混合气体总的物质的量增大、混合气体的温度升高,容器的容积不变,根据pV=nRT判断;
C、反应混合物都是气体,根据质量守恒定律判断;
D、混合气体总的物质的量增大,根据M=
判断;
A、二氧化氮的浓度增大,颜色加深;
B、升高温度,化学平衡向左移动,混合气体总的物质的量增大、混合气体的温度升高,容器的容积不变,根据pV=nRT判断;
C、反应混合物都是气体,根据质量守恒定律判断;
D、混合气体总的物质的量增大,根据M=
| m |
| n |
解答:
解:升高温度,化学平衡向着吸热方向进行,所以化学平衡2NO2?N2O4向左进行.
A、二氧化氮的浓度增大,颜色加深,故A不符合;
B、升高温度,化学平衡向左移动,混合气体总的物质的量增大、混合气体的温度升高,容器的容积不变,根据pV=nRT可知,容器内压强增大,故B不符合;
C、反应混合物都是气体,根据质量守恒定律,混合气体总的质量不变,故C符合;
D、混合气体总的物质的量增大,混合气体总的质量不变,根据M=
可知,混合气体的平均相对分子质量减小,故D不符合;
故选C.
A、二氧化氮的浓度增大,颜色加深,故A不符合;
B、升高温度,化学平衡向左移动,混合气体总的物质的量增大、混合气体的温度升高,容器的容积不变,根据pV=nRT可知,容器内压强增大,故B不符合;
C、反应混合物都是气体,根据质量守恒定律,混合气体总的质量不变,故C符合;
D、混合气体总的物质的量增大,混合气体总的质量不变,根据M=
| m |
| n |
故选C.
点评:本题考查学生温度对化学平衡的影响知识,难度不大,注意根据平衡移动原理理解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中铝元素的质量与溶液中所含铝元素的质量相等,则原氯化铝溶液和氢氧化钠溶液的物质的量浓度之比可能是( )
| A、1:3 | B、3:2 |
| C、1:4 | D、2:7 |
NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、7.8g Na2O2中含有的阴离子数目为0.2NA |
| B、3.2g O2和O3的混合气中含有的氧原子数目为0.2NA |
| C、1L 0.1mol/L的Al2(SO4)3溶液中,Al3+的数目为0.2NA |
| D、过氧化氢分解制得标准状况下1.12L O2,转移电子数目为0.2NA |
下列说法不正确的是( )
| A、豆科植物通过根瘤菌吸收空气中的氮是化学变化 |
| B、汽车尾气中排放的氮氧化合物是由游离态氮转化来的 |
| C、化石燃料燃烧通常不释放出氮氧化合物 |
| D、植物秸秆燃烧时放出氮氧化合物,参与了氮的循环 |
将NaCl和另一氯化物的混合物共1.170g溶于水,然后跟足量的AgNO3 溶液反应,可生成沉淀3.120g.若另一种氯化物为下列四种之一,则不可能是( )
| A、AlCl3 |
| B、MgCl2 |
| C、CaCl2 |
| D、KCl |
aXn+和bYm-两种离子,其电子层结构相同.下列关系式或化学式正确的是( )
| A、a+n=b-m |
| B、b-a=n+m |
| C、氧化物为YOm |
| D、氢化物为YHm |
某原子的相对原子质量是31,原子核外有三个电子层,最外层有5个电子,则该元素原子核中的中子数是( )
| A、12个 | B、15个 |
| C、16个 | D、17个 |
“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体,如图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子.下列说法正确的是( )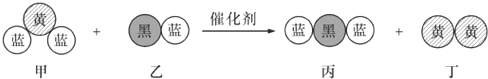

| A、该反应属于置换反应 |
| B、化学方程式中乙、丙的化学计量数均为4 |
| C、甲和丁中同种元素化合价相等 |
| D、甲和丙中所含元素种类相同 |