题目内容
高锰酸钾在不同的条件下发生的反应如下:
① MnO4-+5e-+8H+ ═ Mn2++4H2O
② MnO4-+3e-+2H2O ═ MnO2↓+4OH-
③ MnO4-+e- ═ MnO42- (溶液绿色)
⑴ 从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的____________影响。
⑵ 将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为 __________→___________。
⑶ 将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法正确的是________。
a.氧化性:PbO2 > KMnO4 b.还原性:PbO2 > KMnO4 c.该反应可以用盐酸酸化
⑷ 将高锰酸钾逐滴加入到强碱性硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3∶2,完成下列化学方程式(横线上填系数,括号内填物质),并用单线桥法表示电子的转移情况。
① _______KMnO4+_______K2S+_______( ) ═ ________K2MnO4+________K2SO4+________S↓+________( )。
② 若生成6.4g单质硫,反应过程中转移电子数为____________。
⑸ 已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:
MnO4-→Mn2+; Fe3+→Fe2+; IO3-→I2; HNO3→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是________。
a.MnO4- b.Fe3+ c.IO3- d.HNO3
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案下列有关实验的操作正确的是
实验 | 操作 | |
A. | 配制稀硫酸 | 先将浓硫酸加入烧杯中,后倒入蒸馏水 |
B. | 排水收集KMnO4分解产生的O2 | 先熄灭酒精灯,后移出导管 |
C. | 浓盐酸与MnO2反应制备纯净Cl2 | 气体产物先通过浓硫酸,后通过饱和食盐水 |
D. | CCl4萃取碘水中的I2 | 先从分液漏斗下口放出有机层,后从上口倒出水层 |



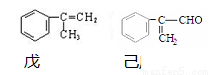
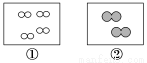
 ”和“
”和“ ”分别表示氢原子和氧原子,则下列说法正确的是( )
”分别表示氢原子和氧原子,则下列说法正确的是( )