题目内容
(21分)2012年8月24日,武汉市一家有色金属制造厂发生氨气泄露事故。已知在一定温度下,合成氨工业原料气H2制备涉及下面的两个反应:
C(s)+H2O(g) 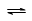 CO(g)+H2(g);
CO(g)+H2(g);
CO(g)+H2O(g)  H2(g)+CO2(g)。
H2(g)+CO2(g)。
(1)判断反应CO(g)+H2O(g) 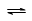 CO2(g)+H2(g)达到化学平衡状态的依据是_____ ___。
CO2(g)+H2(g)达到化学平衡状态的依据是_____ ___。
A.容器内压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(2)在2 L定容密闭容器中通入1 mol N2(g)和3 mol H2(g),发生反应:3H2(g)+N2(g) 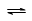 2NH3(g),ΔH<0,测得压强-时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
2NH3(g),ΔH<0,测得压强-时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
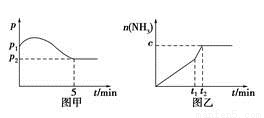
①若图中c=1.6 mol,则改变的条件是________(填字母);
②若图中c<1.6 mol,则改变的条件是_ __(填字母);此时该反应的平衡常数_____(填“增大”、“减小”、“不变”)
A.升温 B.降温 C.加压 D.减压 E.加催化剂
(3)如图甲,平衡时氢气的转化率为________。
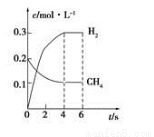
(4)工业上可利用如下反应:H2O (g)+CH4 (g)  CO(g)+3H2(g)制备CO和H2。在一定条件下1 L的密闭容器中充入0.3 mol H2O和0.2 mol CH4,测得H2(g)和CH4(g)的物质的量浓度随时间变化曲线如下图所示:0~4 s内,用H2 (g)表示的反应速率为____________,用CO(g)表示的反应速率为__________。
CO(g)+3H2(g)制备CO和H2。在一定条件下1 L的密闭容器中充入0.3 mol H2O和0.2 mol CH4,测得H2(g)和CH4(g)的物质的量浓度随时间变化曲线如下图所示:0~4 s内,用H2 (g)表示的反应速率为____________,用CO(g)表示的反应速率为__________。
(1)BC (2) ①E ②A 减小
(3)80% (4)0.075 mol/(L·s) 0.025 mol/(L·s)
【解析】
试题分析:(1)A、反应前后气体的物质的量不变,温度一定,容器中压强始终不变,故压强不变,不能说明到达平衡状态,故A错误;B、反应达到平衡状态时,各物质的浓度不变,混合气体中c(CO)不变说明到达平衡状态,故B正确;C、v (H2)正=v (H2O)逆,不同物质表示的速率之比等于化学计量数之比,说明到达平衡状态,故C正确;D、平衡时二氧化碳与一氧化碳的浓度与转化率有关,c(CO2)=c(CO)不能说明到达平衡,故D错误。
(2) 设转化的N2物质的量为x,3H2(g)+N2(g)?2NH3(g),
投料 3mol 1 mol 0
转化量 3x x 2 x
平衡量 3-3x 1-x 2x
反应前后的压强比等于物质的量比,即(4-2x):4=0.6,解得x=0.8mol。
①若图中c=1.6mol,则平衡没移动,但速率加快,所以改变的条件是使用催化剂, 则E项正确。
②若图中c<1.6mol,则平衡逆向移动,且速率加快,只能升高温度;该反应正反应为放热反应,升高温度平衡向吸热的方向移动,即逆向移动,所以平衡常数减小。
(3) 3H2(g)+N2(g)?2NH3(g),
投料 3mol 1 mol 0
转化量 3x x 2x
平衡量 3-3x 1-x 2x
反应前后的压强比等于物质的量比即(4-2x):4=0.6,x=0.8,所以平衡时氢气的转化率为2.4mol÷3mol×100%=80%。
(4)v(H2)=0.3mol/L÷4s=0.075 mol/(L·s),而v(CO)=v(CH4)=0.1mol/L÷4s=0.025 mol/(L?s)。
考点:本题考查化学反应速率、化学平衡的判断、化学平衡移动、图像的分析、化学平衡的计算。

 阅读快车系列答案
阅读快车系列答案

 >X?>HCO
>X?>HCO
 Sr2+(aq)+SO
Sr2+(aq)+SO (aq) Ksp=2.5×10-7
(aq) Ksp=2.5×10-7 (aq) Ksp=2.5×10-9
(aq) Ksp=2.5×10-9