题目内容
在一固定容积为2L的密闭容器中加入2mol A和3mol B,保持温度为30℃,在催化剂存在的条件下进行下列反应:2A(g)+3B(g)═3C(g),2分钟达到平衡,生成1.5mol C,此时,平衡混合气中C的体积分数为ω1;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1mol,体积分数为ω2,请回答下列问题,
(1)该反应在30℃时平衡常数K1= ,焓变△H 0(填“>”、“<”或“=”).
(2)该反应在30℃时平衡混合气中C的体积分数为ω1= ;从反应开始到达到化学平衡状态时v(A)=
(3)该反应在70℃时平衡常数为K2,则 K1 K2(填“>”、“=”或“<”)
(1)该反应在30℃时平衡常数K1=
(2)该反应在30℃时平衡混合气中C的体积分数为ω1=
(3)该反应在70℃时平衡常数为K2,则 K1
考点:化学平衡的计算,化学平衡常数的含义
专题:化学平衡专题
分析:(1)2min达平衡,平衡时C为1.5mol,据此利用三段式计算平衡时各组分的平衡浓度,代入平衡常数表达式计算;
由题意可知,升高温度平衡时C的物质的量增大,说明升高温度平衡向正反应移动,故正反应为吸热反应;
(2)根据平衡时C的物质的量,利用差量法计算反应混合物减少的物质的量,进而计算平衡时反应混合物的总的物质的量,再根据体积分数定义计算;
根据v=
计算v(C),再利用速率之比等于化学计量数之比计算v(A);
(3)升高温度平衡向正反应方向移动,说明温度越高平衡常数越大.
由题意可知,升高温度平衡时C的物质的量增大,说明升高温度平衡向正反应移动,故正反应为吸热反应;
(2)根据平衡时C的物质的量,利用差量法计算反应混合物减少的物质的量,进而计算平衡时反应混合物的总的物质的量,再根据体积分数定义计算;
根据v=
| ||
| △t |
(3)升高温度平衡向正反应方向移动,说明温度越高平衡常数越大.
解答:
解:(1)2min达平衡,平衡时C为1.5mol,C的平衡浓度为
=0.75mol/L,则:
2A(g)+3B(g)?3C(g)
开始(mol/L):1 1.5 0
变化(mol/L):0.5 0.75 0.75
平衡(mol/L):0.5 0.75 0.75
故30℃平衡常数k=
=4,
由题意可知,升高温度平衡时C的物质的量增大,说明升高温度平衡向正反应移动,故正反应为吸热反应,即△H>0,
故答案为:4;>;
(2)30℃时平衡时C的物质的量为1.5mol,则:
2A(g)+3B(g)?3C(g)物质的量减少△n
3 2
1.5mol 1mol
故平衡时反应混合物总的物质的量为2mol+3mol-1mol=4mol,C的体积分数ω1=
×100%=37.5%,
v(C)=
=0.375mol/(L?min),速率之比等于化学计量数之比,所以v(A)=
v(C)=
×0.375mol/(L?min)=0.25mol/(L?min),
故答案为:37.5%;0.25mol/(L?min);
(3)升高温度平衡向正反应方向移动,说明温度越高平衡常数越大,故K1<K2,故答案为:<.
| 1.5mol |
| 2L |
2A(g)+3B(g)?3C(g)
开始(mol/L):1 1.5 0
变化(mol/L):0.5 0.75 0.75
平衡(mol/L):0.5 0.75 0.75
故30℃平衡常数k=
| 0.75 3 |
| 0.52×0.75 3 |
由题意可知,升高温度平衡时C的物质的量增大,说明升高温度平衡向正反应移动,故正反应为吸热反应,即△H>0,
故答案为:4;>;
(2)30℃时平衡时C的物质的量为1.5mol,则:
2A(g)+3B(g)?3C(g)物质的量减少△n
3 2
1.5mol 1mol
故平衡时反应混合物总的物质的量为2mol+3mol-1mol=4mol,C的体积分数ω1=
| 1.5mol |
| 4mol |
v(C)=
| ||
| 2min |
| 2 |
| 3 |
| 2 |
| 3 |
故答案为:37.5%;0.25mol/(L?min);
(3)升高温度平衡向正反应方向移动,说明温度越高平衡常数越大,故K1<K2,故答案为:<.
点评:本题考查化学平衡的有关计算、化学平衡常数、平衡状态的判断、反应速率的计算等,题目综合性较大,难度中等,注意基础知识的理解掌握

练习册系列答案
 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案
相关题目
下列实验设计方案中,可行的是( )
| A、用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体 |
| B、在某试样中加入NaOH溶液加热,产生能使蓝色石蕊试纸变红的气体即证明有NH4+ |
| C、焰色反应实验中用硫酸清洗铁丝,灼烧后再沾取试样在酒精灯上灼烧观察 |
| D、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
在可逆反应2A(g)+3B(g)?xC(g)+D(g)中,已知:反应开始加入的物质只有A、B,起始浓度A为5mol?L-1,B为3mol?L-1,前2min C的平均反应速率为0.5mol?L-1?min-1.2min后,测得D的浓度为0.5mol?L-1.(设反应前后溶液体积不变)则关于此反应的下列说法中正确的是( )
| A、2 min末时A和B的浓度之比为2:3 |
| B、x=1 |
| C、2 min末时B的转化率为50% |
| D、2 min时A的消耗浓度为4mol?L-1 |
已知在常温下可以发生下列反应:H2SO3+I2+H2O=4H++2I-+SO42-2Fe3++2I-=2Fe2++I23Fe2++4H++NO-=3Fe3++NO+2H2O则有关物质的还原性由强到弱的顺序是( )
| A、H2SO3>I->Fe2+>NO |
| B、I->Fe2+>H2SO3>NO |
| C、Fe2+>I->H2SO3>NO |
| D、NO>Fe2+>I->H2SO3 |

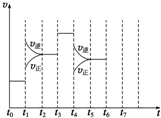 在一密闭容器中发生反应N2+3H2?2NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
在一密闭容器中发生反应N2+3H2?2NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示: