题目内容
某氨水的pH=a,其中水的电离度为α1;某硝酸的pH=b,其中水的电离度为α2;已知a+b=14,a>11.将氨水与硝酸等体积混合后,所得溶液中水的电离度为α3.相同条件下纯水的电离度为α4.则下列关系中正确的是( )
| A、α3>α4>α2=α1 |
| B、α4>α3>α2=α1 |
| C、c(NO3-)>c(NH4+)>c(OH-)>c(H+) |
| D、c(NO3-)>c(NH4+)>c(H+)>c(OH-) |
考点:离子浓度大小的比较
专题:电离平衡与溶液的pH专题
分析:c(H+)?c(OH-)=KW,纯水溶液中氢离子浓度始终等于氢氧根离子浓度,温度不变,水的离子积常数不变,
常温下,纯水的电离度为α4,水电离出的c(H+)=c(OH-)=10-7mol?L-1;
a+b=14,a>11,可以设氨水溶液的pH=a=12,则b=2,
pH=12的氨水溶液中的氢离子是水电离的,则水电离出的c(H+)=c(OH-)=10-12mol/L,水的电离度为α1;
pH=2的硝酸中c(H+)=10-2mol/L,硝酸溶液中的氢氧根离子是水电离的,根据KW=c(H+)?c(OH-)=10-14,求得水电离出的c(H+)=c(OH-)=10-12mol/L,水的电离度为α2;
pH=2的硝酸和pH=12的氨水等体积混合,NH3?H2O+HCl═NH4Cl+H2O,一水合氨为弱碱,混合液中氨水过量,溶液显示碱性,抑制了水的电离,抑制程度小于原氨水和硝酸,故水的电离程度大小为:α4>α3>α2=α1;
由于混合液为碱性,氨水过量,则溶液中离子浓度大小为:c(NH4+)>c(NO3-)>c(OH-)>c(H+).
常温下,纯水的电离度为α4,水电离出的c(H+)=c(OH-)=10-7mol?L-1;
a+b=14,a>11,可以设氨水溶液的pH=a=12,则b=2,
pH=12的氨水溶液中的氢离子是水电离的,则水电离出的c(H+)=c(OH-)=10-12mol/L,水的电离度为α1;
pH=2的硝酸中c(H+)=10-2mol/L,硝酸溶液中的氢氧根离子是水电离的,根据KW=c(H+)?c(OH-)=10-14,求得水电离出的c(H+)=c(OH-)=10-12mol/L,水的电离度为α2;
pH=2的硝酸和pH=12的氨水等体积混合,NH3?H2O+HCl═NH4Cl+H2O,一水合氨为弱碱,混合液中氨水过量,溶液显示碱性,抑制了水的电离,抑制程度小于原氨水和硝酸,故水的电离程度大小为:α4>α3>α2=α1;
由于混合液为碱性,氨水过量,则溶液中离子浓度大小为:c(NH4+)>c(NO3-)>c(OH-)>c(H+).
解答:
解:a+b=14、a>11,可以设氨水溶液的pH=a=12,则硝酸溶液的pH=b=2,
pH=12的氨水溶液中的氢离子是水电离的,则水电离出的c(H+)=c(OH-)=10-12mol/L,水的电离度为α1;
pH=2的硝酸中c(H+)=10-2mol/L,硝酸溶液中的氢氧根离子是水电离的,根据KW=c(H+)?c(OH-)=10-14,求得水电离出的c(H+)=c(OH-)=10-12mol/L,水的电离度为α2;
pH=2的硝酸和pH=12的氨水等体积混合,NH3?H2O+HCl═NH4Cl+H2O,一水合氨为弱碱,混合液中氨水过量,溶液显示碱性,抑制了水的电离,抑制程度小于原氨水和硝酸,
常温下,纯水的电离度为α4,水电离出的c(H+)=c(OH-)=10-7mol?L-1;
所以水的电离度大小为:α4>α3>α2=α1,故B正确;
由于混合液中氨水过量,溶液为碱性,则c(OH-)>c(H+),根据电荷守恒可得:c(NH4+)>c(NO3-),所以溶液中离子浓度大小为:c(NH4+)>c(NO3-)>c(OH-)>c(H+),故C、D错误;
故选B.
pH=12的氨水溶液中的氢离子是水电离的,则水电离出的c(H+)=c(OH-)=10-12mol/L,水的电离度为α1;
pH=2的硝酸中c(H+)=10-2mol/L,硝酸溶液中的氢氧根离子是水电离的,根据KW=c(H+)?c(OH-)=10-14,求得水电离出的c(H+)=c(OH-)=10-12mol/L,水的电离度为α2;
pH=2的硝酸和pH=12的氨水等体积混合,NH3?H2O+HCl═NH4Cl+H2O,一水合氨为弱碱,混合液中氨水过量,溶液显示碱性,抑制了水的电离,抑制程度小于原氨水和硝酸,
常温下,纯水的电离度为α4,水电离出的c(H+)=c(OH-)=10-7mol?L-1;
所以水的电离度大小为:α4>α3>α2=α1,故B正确;
由于混合液中氨水过量,溶液为碱性,则c(OH-)>c(H+),根据电荷守恒可得:c(NH4+)>c(NO3-),所以溶液中离子浓度大小为:c(NH4+)>c(NO3-)>c(OH-)>c(H+),故C、D错误;
故选B.
点评:本题考查了溶液中离子浓度大小比较、水的电离及其影响因素,题目难度中等,注意掌握酸碱溶液对水的电离程度的影响,明确弱电解质的电离情况,能够根据电荷守恒、盐的水解判断溶液中离子浓度大小.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | 乙烷(乙烯) | 氢气 | 加热 |
| A、A | B、B | C、C | D、D |
对于某合成材料(如塑料制品)废弃物的处理方法中正确的是( )
| A、将废弃物混在垃圾中填埋在土壤中 |
| B、将废弃物焚烧 |
| C、将废弃物用化学方法加工成涂料或汽油 |
| D、将废弃物倾倒在海洋中 |
有关离子浓度大小比较的判断正确的是( )
| A、常温下NaB溶液的pH=8,c(Na+)-c(B-)=1×10-2 mol/L |
| B、Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、KHSO3溶液呈酸性,c(K+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-) |
| D、0.1mol?L-1 NH4Cl和0.1mol?L-1 NH3?H2O等体积混合后溶液呈碱性:c(NH3?H2O)>c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
单糖是( )
| A、具有甜味的物质 |
| B、具有一个分子比较简单的糖 |
| C、不能在水解成更简单的糖 |
| D、最简式为的Cn(H2O)m有机物 |
已知分子式为C10H14的分子,不能使溴水褪色,但可使酸化的高锰酸钾溶液褪色.它的分子结构中含有一个烷基,它与液溴在还原铁粉存在下,反应生成物结构有3种,则此烷基的结构有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
下列离子中,核外有10个电子的是( )
| A、Mg2+ |
| B、S2- |
| C、K+ |
| D、Cl- |
升高温度,下列数据不一定增大的是( )
| A、化学反应速率v |
| B、弱电解质的电离平衡常数Ka |
| C、化学平衡常数K |
| D、水的离子积常数KW |
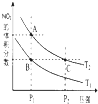 氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.