题目内容
N、S、K、Fe是四种常见的元素.
(1)Fe在周期表中的位置是 ;N基态原子有 个未成对电子;S基态原子电子排布式是 .
(2)在催化剂存在下,NH3可用来消除NO的污染,生成2种对环境无害的物质.写出该反应的化学方程式: ;该反应中氧化产物与还原产物的物质的量之比为 .
(3)16g S完全燃烧放出热量148.5kJ,硫燃烧热的热化学方程式为: .
(1)Fe在周期表中的位置是
(2)在催化剂存在下,NH3可用来消除NO的污染,生成2种对环境无害的物质.写出该反应的化学方程式:
(3)16g S完全燃烧放出热量148.5kJ,硫燃烧热的热化学方程式为:
考点:原子核外电子排布,氧化还原反应,热化学方程式
专题:
分析:(1)根据Fe元素的质子数可知电子数为26,核外各电子层电子数为2、8、14、2,所以位于第四周期第VIII族;根据N原子的价层电子排布式分析未成对电子;S元素为16号元素,原子核外有16个电子,据核外电子排布规律书写;
(2)NH3可用来消除NO的污染,生成2种对环境无害的物质,应生成氮气和水;
(3)计算出硫的物质的量,可计算出1molS燃烧放出的热量,进而书写热化学方程式.
(2)NH3可用来消除NO的污染,生成2种对环境无害的物质,应生成氮气和水;
(3)计算出硫的物质的量,可计算出1molS燃烧放出的热量,进而书写热化学方程式.
解答:
解:(1)根据Fe元素的质子数可知电子数为26,核外各电子层电子数为2、8、14、2,其原子基态时的核外电子排布式为1s22s22p63s23p63d64s2,所以位于第四周期第VIII族;
N原子的价层电子排布式为2s22p3,p能级有3个简并轨道,3个电子分别占据1个轨道,且自旋方向相同,有3个未成对电子;
S元素为16号元素,原子核外有16个电子,所以核外电子排布式为:1s22s22p63s23p4;
故答案为:第4周期Ⅷ族;3;1s22s22p63s23p4;
(2)NH3可用来消除NO的污染,生成2种对环境无害的物质,应生成氮气和水,反应的方程式为4NH3+6NO
5N2+6H2O,反应中只有N元素化合价发生变化,由方程式可知反应中氧化产物与还原产物的物质的量之比为4:6=2:3,
故答案为:4NH3+6NO
5N2+6H2O;2:3;
(3)n(S)=
=0.5mol,则1molS完全燃烧放出的热量为148.5kJ×2=297kJ,则热化学方程式为S(s)+O2(g)=SO2(g);△H=-297kJ/mol,
故答案为:S(s)+O2(g)=SO2(g);△H=-297kJ/mol.
N原子的价层电子排布式为2s22p3,p能级有3个简并轨道,3个电子分别占据1个轨道,且自旋方向相同,有3个未成对电子;
S元素为16号元素,原子核外有16个电子,所以核外电子排布式为:1s22s22p63s23p4;
故答案为:第4周期Ⅷ族;3;1s22s22p63s23p4;
(2)NH3可用来消除NO的污染,生成2种对环境无害的物质,应生成氮气和水,反应的方程式为4NH3+6NO
| ||
| △ |
故答案为:4NH3+6NO
| ||
| △ |
(3)n(S)=
| 16g |
| 32g/mol |
故答案为:S(s)+O2(g)=SO2(g);△H=-297kJ/mol.
点评:本题考查较为综合,涉及多方面的知识,侧重考查了核外电子排布规律、元素在周期表位置的判断、热化学方程式的书写,为高考常题型和高频考点,注意基态原子的核外电子排布式,注意相关知识的积累,题目难度中等.

练习册系列答案
相关题目
稀释某弱酸HA溶液时,浓度增大的是( )
| A、HA |
| B、H+ |
| C、A- |
| D、OH- |
恒温、恒压下,1mol A和n mol B在一个容积可变的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成a mol C.则下列说法正确的是( )
| A、物质A的转化率为a | ||
B、起始时刻和达到平衡时容器中的压强比为(1+n):(1+n-
| ||
| C、反应达平衡后,再向容器中充入amolHe,物质B的转化率减小 | ||
| D、当v正(A)=2v逆(C)时,可判断反应达到平衡 |
现用pH=3的CH3COOH溶液和pH=11的NaOH溶液各V mL,进行中和滴定,当滴定到pH=7时,锥形瓶内溶液的体积为(滴定前后溶液未稀释、总体积不变)( )
| A、等于2V mL |
| B、小于2V mL |
| C、大于2V mL |
| D、无法确定 |
下列有关实验原理或实验操作正确的是( )
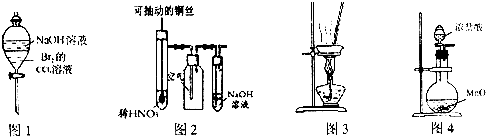

| A、图1装置可以用于除去溶解在CCl4中的Br2 |
| B、图2所示装置微热稀HNO3,在广口瓶中可收集NO气体 |
| C、用图3装置在蒸发皿中灼烧CuSO4?5H2O晶体以除去结晶水 |
| D、实验室常用图4装置制取少量氯气 |
下列行为中,符合安全要求的是( )
| A、金属钠意外着火时,立即用沾水的毛巾覆盖 |
| B、当有大量氯气泄漏时,人应沿顺风方向疏散 |
| C、将含有硫酸的废液倒入水池,用大量水冲入下水道 |
| D、严禁在加油站附近放烟花爆竹 |