题目内容
5.(1)铜既能与稀硝酸反应.也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3═Cu(NO3)2+NO↑+NO2↑+H2O (未配平)
①硝酸在该反应中的作用是氧化性和酸性,
②19.2g Cu被硝酸完全溶解后,若得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是0.9mol.
(2)①已知白磷和氯酸溶液可发生如下反应:
□P4+□HClO3+□18H2O═□HCl+□H3PO4
配平上述反应方程式,并表示电子转移的方向和数目.
②白磷有毒,有实验室可采用CuSO4溶液进行处理,其反应为:
11P4+60CuSO4+96H2O═20Cu3P+24H3PO4+60H2SO4
在该反应中30mol CuSO4可氧化P4的物质的量是1.5mol.
(3)新型纳米材料氧缺位铁酸锌(ZnFe2Ox),常温下它能使工业废气中的氮的氧化物、SO2等分解,减小工业废气对环境的影响,它可由铁酸锌(ZnFe2O4)经高温还原制得.转化流程如图所示:
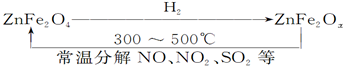
若2mol ZnFe2Ox与SO2可生成0.75mol S,x=3.25.写出铁酸锌高温被H2还原生成氧缺位铁酸锌的化学方程式4ZnFe2O4+3H2$\frac{\underline{\;高温\;}}{\;}$4ZnFe2O3.25+3H2O.
分析 (1)①该反应硝酸中部分N元素化合价由+5价变为+2、+4价,部分N元素化合价不变,据此判断硝酸性质;
②利用电子守恒来计算作氧化剂的硝酸的物质的量,作酸性和作氧化剂的物质的量之和为参加反应的硝酸的物质的量;
(2)①该反应中P元素化合价由0价变为+5价、Cl元素化合价由+5价变为-1价,根据转移电子守恒及原子守恒配平方程式;
②根据转移电子守恒计算硫酸铜氧化白磷的物质的量;
(3)根据得失电子守恒和化学式中元素化合价代数和为零计算,铁酸锌高温下被氢气还原生成氧缺位铁酸锌和水.
解答 解:(1)①该反应硝酸中部分N元素化合价由+5价变为+2、+4价,部分N元素化合价不变,所以硝酸体现氧化性和酸性,故答案为:氧化性和酸性;
②n(Cu)=$\frac{19.2g}{64g/mol}$=0.3mol,
设NO的物质的量为n,得到的NO和NO2物质的量相同,
由电子守恒可知,0.3mol×2=n×(5-2)+n×(5-4),
解得n=0.15mol,
由N原子守恒可知作氧化剂的硝酸为0.15mol+0.15mol=0.3mol,
由Cu(NO3)2可知,作酸性的硝酸为0.3mol×2=0.6mol,
则参加反应的硝酸的物质的量是0.3mol+0.6mol=0.9mol,
故答案为:0.9mol;
(2)①反应中P元素的化合价由0价升高到+5价,Cl元素的化合价由+5价降低到-1价,根据得失电子数目相等可知二者计量数之比为3:10,则结合质量守恒定律可知平衡后的化学方程式为3P4+10HClO3+18H2O=10HCl+12H3PO4,
故答案为:3;10;18H2O;10;12;
②30mol硫酸铜转移电子物质的量=30mol×(2-0)=60mol,氧化白磷物质的量=$\frac{60mol}{4×(5-0)}$=1.5mol,故答案为:1.5mol;
(3)新型纳米材料ZnFe2OX可由化合物ZnFe2O4经高温还原制得,若2mol ZnFe2OX与SO2反应可生成0.75molS,则ZnFe2OX被还原为ZnFe2O4,令中铁元素的化合价为a,根据电子转移守恒,可知2mol×2×(3-a)=0.75mol×4,解得,a=2.25,利用化合价代数和为零,2+2.25×2=2x,解得x=3.25,
铁酸锌高温下被氢气还原生成氧缺位铁酸锌和水,该反应为4ZnFe2O4+3H2 $\frac{\underline{\;高温\;}}{\;}$4ZnFe2O3.25+3H2O,
故答案为:3.25;4ZnFe2O4+3H2$\frac{\underline{\;高温\;}}{\;}$4ZnFe2O3.25+3H2O.
点评 本题涉及氧化还原反应计算、化学方程式的配平等知识点,较综合,把握题干中信息及发生的化学反应是解本题关键,题目难度较大.

| A. | 氯气是无色、有刺激性气味的有毒气体 | |
| B. | 氯气在常压下冷却到-34.6℃变成液氯,它是易液化的气体之一 | |
| C. | 氢气在氯气中燃烧火焰呈淡蓝色 | |
| D. | 红热的铜丝放人氯气中生成绿色的氯化铜 |
| A. | 稀硫酸 | B. | 乙醇 | C. | 稀硝酸 | D. | 氢氧化钠溶液 |
a Fe2++b Br-+c Cl2→d Fe3++e Br2+f Cl-
下列选项中的数字与离子方程式中的a.b.c.d.e.f一一对应,其中不符合反应实际的是( )
| A. | 2 4 3 2 2 6 | B. | 0 2 1 0 1 2 | ||
| C. | 2 0 1 2 0 2 | D. | 2 2 2 2 1 4 |
| A. | 30mL | B. | 55mL | C. | 65mL | D. | 175mL |
| A. | 放电时,负极反应为2n-2e-+20H一═Zn(OH)2 | |
| B. | 充电时,阴极pH增大 | |
| C. | 放电时,若有6mol电子转移,则正极有10 mol OH一移向负极 | |
| D. | 充电时,阳极反应为Fe(OH)3+50H一+3e一=Fe042-+4H20 |
| A. | 两元素均位于元素周期表中第4周期Ⅷ族 | |
| B. | 两者均能被潮湿空气腐蚀 | |
| C. | 氧化性:Cu2+>Fe3+>Fe2+ | |
| D. | 铁丝和铜丝在氯气里燃烧均生成二价氯化物 |
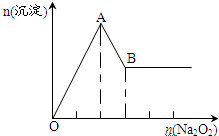 有一透明溶液,可能含有较大量的NH4+、Fe3+、Na+、SO42-、CO32-、H+、Mg2+、Al3+、Cu2+中的某一种或几种,取此溶液做下列试验
有一透明溶液,可能含有较大量的NH4+、Fe3+、Na+、SO42-、CO32-、H+、Mg2+、Al3+、Cu2+中的某一种或几种,取此溶液做下列试验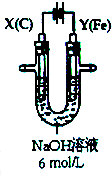 用如图所示装置进行实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.
用如图所示装置进行实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.