题目内容
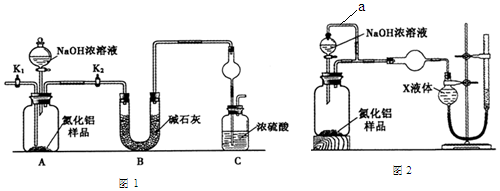
6.在图各物质的相互转化关系中:甲、乙、丙为三种金属单质;A、C、D常温下为气体,其中C呈黄绿色;G为白色沉淀;H为红褐色沉淀;B溶液焰色反应显黄色.(图中部分反应条件及生成物未全部标出)
填写下列空格:
(1)反应①的化学反应方程式2Na+2H2O﹦2NaOH+H2↑
(2)F的化学式FeCl2
(3)写出B溶液与单质乙反应的化学方程式2Al+2OH-+2H2O=2AlO2-+3H2↑
(4)C气体与F溶液反应的离子方程式Cl2+2Fe2+=2Fe3++2Cl-
(5)写出实验室制备C气体的化学方程式MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
分析 甲、乙、丙为三种金属单质;A、C、D常温下为气体,其中C呈黄绿色判断为Cl2;G为白色沉淀;H为红褐色沉淀判断为Fe(OH)3;G为Fe(OH)2,B溶液焰色反应显黄色说明含有钠元素,金属甲和水反应生成气体A和碱B,金属乙和碱反应证明为Al,所以B为NaOH,甲为Na,A为H2,D为HCl,E为盐酸溶液,依据G的成分可知F一定含铁元素,因此丙为Fe,金属铁和盐酸溶液反应生成F为FeCl2,以此解答该题.
解答 解:(1)反应①为钠和水分反应,化学反应方程式为2 Na+2 H2O﹦2NaOH+H2↑,故答案为:2 Na+2 H2O﹦2NaOH+H2↑;
(2)上述推断可知,F为氯化亚铁的化学式为:FeCl2,故答案为:FeCl2;
(3)B为NaOH与乙为Al反应生成A为H2,反应的离子反应方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)C气体与F溶液反应的离子方程式为Cl2+2Fe2+=2 Fe3++2Cl-,故答案为:Cl2+2Fe2+=2 Fe3++2Cl-;
(5)实验室用浓盐酸和二氧化锰在加热条件下制备氯气,方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2 H2O,故答案为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2 H2O.
点评 本题考查无机物的推断,为高考常见题型,侧重考查学生的分析能力,明确物质的颜色及性质是解答本题的关键,注意C、H是解答本题的突破口,并规范化学用语的应用,题目难度不大.

练习册系列答案
相关题目
7.下列说法或表示方法中,正确的是( )


| A. | 等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量少 | |
| B. | 如图可表示C和H2O(g)反应过程中的能量变化 | |
| C. | 吸热反应一定要加热,才能进行 | |
| D. | 已知中和热为57.3 kJ•mol-1,则浓硫酸与NaOH溶液反应生成 1mol H2O时,共放出57.3 kJ的能量 |
14.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 乙酸和乳酸(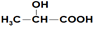 )的混合物共3.0 g,含有的原子总数为0.4 NA )的混合物共3.0 g,含有的原子总数为0.4 NA | |
| B. | 4.6 g乙醇含有-OH数为NA | |
| C. | 1.7 g H2O2中含有的电子数为NA | |
| D. | 1 mol Na2O2固体中含离子总数为4NA |
11.X、Y、Z、R是短周期主族元素,X原子最外层电子数为电子总数的2/3,Y原子最外层电子数是内层电子数的3倍,Z元素的单质常温下能与水反应产生氢气,R原子的核外电子数是X原子与Z原子的核外电子数之和.下列叙述正确的是( )
| A. | 原子半径的大小顺序:X>Y>Z>R | |
| B. | 最高价氧化物的水化物的酸性:R>X | |
| C. | 氢化物的稳定性:X>Y | |
| D. | Y与Z形成的两种化合物中的化学键和晶体类型均相同 |
18.向800mL稀硝酸中加入一定质量的铁粉,铁粉完全溶解后,放出NO气体11.2L(标准状况),同时溶液质量增加18.6g,下列判断正确的是( )
| A. | 原溶液中投入铁粉物质的量是0.5mol | |
| B. | 原溶液中的HNO3浓度是2.0mol•L-1 | |
| C. | 反应后的溶液中c(Fe2+):c(Fe3+)=1:1 | |
| D. | 反应后的溶液中还可以溶解16.0g铜 |
15.铜锌原电池的装置如图所示,下列说法正确的是( )
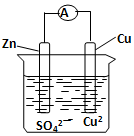

| A. | 锌电极上发生还原反应 | B. | 铜电极上发生氧化反应 | ||
| C. | 铜片上都有氧气产生 | D. | 电流由铜流向锌 |