题目内容
20.某学生配制了100mL 1mol/L的硫酸溶液,在配制过程中,下列操作可能导致溶液浓度偏低的是( )①定容时仰视刻度线
②将浓硫酸在烧杯中稀释,转移到容积为100mL的容量瓶中后,没有洗涤烧杯
③在转移过程中用玻璃棒引流,因操作不慎有少量溶液流到了容量瓶外面
④最后定容时,加水超过了刻度,马上用胶头滴管吸去多余的水,使溶液凹液面刚好与刻度线相切.
| A. | ②③④ | B. | ③④ | C. | ①②③④ | D. | ①②③ |
分析 根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析,凡是不当操作使n偏小或者使V偏大的操作都会使溶液浓度偏低,凡是不当操作使n偏大或者使V偏小的操作都会使溶液浓度偏高,据此解答.
解答 解:①定容时仰视刻度线,导致溶液体积偏大,溶液浓度偏低,故选;
②将浓硫酸在烧杯中稀释,转移到容积为100mL的容量瓶中后,没有洗涤烧杯,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故选;
③在转移过程中用玻璃棒引流,因操作不慎有少量溶液流到了容量瓶外面,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故选;
④最后定容时,加水超过了刻度,马上用胶头滴管吸去多余的水,使溶液凹液面刚好与刻度线相切,导致溶质部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故选;
故选:C.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,准确判断不当操作对溶质的物质的量和溶液体积的影响是解题关键,题目难度不大.

练习册系列答案
相关题目
10.下列化学反应中有电子得失的是( )
| A. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | B. | N2+3H2$?_{催化剂}^{高温、高压}$2NH3 | ||
| C. | Mg+Cl2$\frac{\underline{\;点燃\;}}{\;}$MgCl2 | D. | NaHCO3+HCl=NaCl+CO2↑+H2O |
8.近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好.如图是以烃A为原料生产人造羊毛的合成路线.下列说法正确的是( )
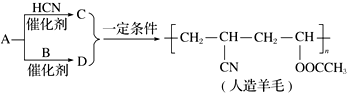

| A. | 合成人造羊毛的反应属于缩聚反应 | B. | A生成C的反应属于加成反应 | ||
| C. | A生成D的反应属于取代反应 | D. | 烃A的结构简式为CH2═CH2 |
15.下列分子的立体结构模型正确的是( )
| A. | CO2的立体结构模型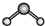 | B. | PH3的立体结构模型 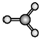 | ||
| C. | H2S的立体结构模型 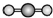 | D. | CH4的立体结构模型 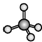 |
9.下列离子方程式不正确的是( )
| A. | 铁粉投入FeCl3溶液中 Fe+2Fe3+=2Fe2+ | |
| B. | 碳酸钙与盐酸反应 CO32-+2H+=H2O+CO2↑ | |
| C. | 氢氧化钠溶液与稀硫酸反应 H++OH-=H2O | |
| D. | 铁与盐酸反应 2Fe+6H+=2Fe3++3H2↑ |
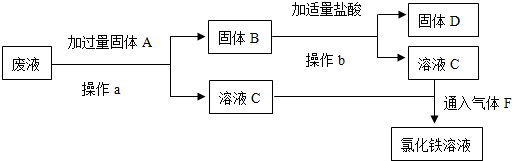
 实验室需要配制0.50mol/L NaCl溶液480mL.
实验室需要配制0.50mol/L NaCl溶液480mL.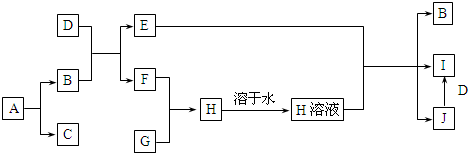 请回答下列问题:
请回答下列问题: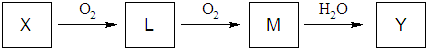
 ,则该有机物核磁共振氢谱有3 个峰.
,则该有机物核磁共振氢谱有3 个峰.