题目内容
16.下列有关叙述正确的是( )| A. | BaCO3难溶于水中,可用作X射线透视肠胃的内服药 | |
| B. | 中国在建的第二艘航母中使用的碳纤维是一种新型的有机高分子材料 | |
| C. | 酸碱指示剂变色、煤的液化、蛋白质的颜色反应、海水提取溴、焰色反应都涉及化学变化 | |
| D. | 获得2015年诺贝尔医学奖的屠呦呦用乙醚从黄花蒿中提取出青蒿素,该技术应用了萃取原理 |
分析 A.碳酸钡易溶于盐酸;
B.碳纤维为无机物;
C.化学变化一定有新物质生成;
D.青蒿素易溶于乙醚,用乙醚从青蒿中提取青蒿素,用到了萃取原理.
解答 解:A.碳酸钡易溶于盐酸,与盐酸反应生成易溶性氯化钡,钡离子为重金属离子,能够使人体中毒,故A错误;
B.碳纤维为无机物,不属于新型的有机高分子材料,故B错误;
C.焰色反应是元素的性质,焰色反应属于物理变化,故C错误;
D.青蒿素易溶于乙醚,用乙醚从青蒿中提取青蒿素,用到了萃取原理,故D正确;
故选:D.
点评 本题考查物质的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,把握相关物质的结构和性质,为解答该类题目的关键,难度不大,注意物理变化与化学变化的区别.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列叙述正确的是( )
| A. | 阳离子一定是金属离子,阴离子一定只含非金属元素 | |
| B. | 金属阳离子一定只具有氧化性,没有还原性 | |
| C. | 阴、阳离子相互作用后不一定形成离子化合物 | |
| D. | 金属和非金属化合一定生成离子化合物 |
4.在元素Fe单质及其化合物变化中,下列说法正确的是( )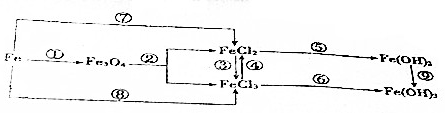

| A. | ③反应的离子方程式为2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 钢铁腐蚀时,负极发生的反应是Fe-3e-═Fe3+ | |
| C. | 以Fe为电极,电解饱和NaCl溶液,阳极反应式为2Cl--2e-═Cl2↑ | |
| D. | FeCl2溶液中混有少量FeCl3,可以加入Fe、Cu等金属除去FeCl3 |
8.下列各组离子在溶液中能大量共存,且加入铝粉一定能放出氢气的是( )
| A. | Fe2+、Na+、H+、SO42- | B. | H+、Ba2+、Cl-、NO3- | ||
| C. | Ba2+、Na+、OH-、SO42- | D. | Na+、Mg2+、NO3-、OH- |
5.下列反应中,属于氧化还原反应的是( )
| A. | CaO+2HCl=CaCl2+H2O | B. | CaO+H2O=Ca(OH)2 | ||
| C. | CaCO3=CaO+CO2↑ | D. | 2 H2O2=2H2O+O2↑ |
6.镁-次氯酸盐燃料电池的工作原理如图所示,该电池反应为:Mg+ClO-+H2O=Mg(OH)2+Cl-,下列有关说法正确的是( )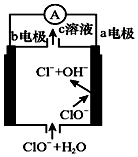

| A. | 电池工作时,c溶液中的溶质一定是MgCl2 | |
| B. | 负极反应式:ClO--2e-+H2O=Cl-+2OH- | |
| C. | 电池工作时,OH-向b电极移动 | |
| D. | b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl- |