题目内容
5.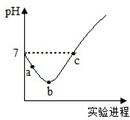 室温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液.整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是( )
室温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液.整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是( )| A. | 实验进程中可用pH试纸测定溶液的pH | |
| B. | c点所示溶液中:c(Na+)=2c(ClO-)+c(HClO) | |
| C. | 向a点所示溶液中通入SO2,溶液的酸性和漂白性均增强 | |
| D. | 由a点到b点的过程中,溶液中$\frac{c(Cl{O}^{-})}{c({H}^{+})}$增大 |
分析 整个过程发生的反应为Cl2+H2O═HCl+HClO、HCl+NaOH═NaCl+H2O、HClO+NaOH═NaClO+H2O,根据溶液的酸碱性结合电荷守恒和物料守恒分析解答.
解答 解:A.溶液中含有次氯酸,具有漂白性,不能用pH试纸测量,故A错误;
B.c点溶液呈中性,则c(H+)=c(OH-),根据电荷守恒得c(H+)+c(Na+)=c(Cl-)+c(Cl0-)+c(OH-),所以c(Na+)=c(Cl-)+c(ClO-),根据物料守恒得c(Cl-)=c(ClO-)+c(HClO),所以c(Na+)=c(HClO)+2c(ClO-),故B正确;
C.氯气具有氧化性,能将二氧化硫氧化为硫酸,自身被还原为盐酸,所得到的溶液不再具有漂白性,但酸性增强,故C错误;
D.由a点到b点的过程是氯气的溶解平衡Cl2+H2O?H++Cl-+HClO向右进行的过程,酸性逐渐增强,氢离子浓度逐渐增大,溶液中$\frac{c(Cl{O}^{-})}{c({H}^{+})}$减小,故D错误.
故选B.
点评 本题综合考查氯气的性质,侧重于学生的分析能力的考查,注意理解溶液中的溶质及其性质是解本题关键,根据物料守恒得c(Cl-)=c(ClO-)+c(HClO),为易错点,题目难度中等.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
16.下列离子组合,能够大量共存的是( )
| A. | 酸性溶液中:Al3+、Fe3+、SO42-、SCN- | |
| B. | 透明溶液中:MnO4-、K+、Na+、NO3- | |
| C. | 强碱性溶液中:Na+、NO3-、HCO3-、SO32- | |
| D. | 强酸性溶液中:Na+、Fe2+、SO42-、NO3- |
13.若NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A. | 标准状况下,22.4 L H2和Cl2的混合气体中含有的分子数为2NA | |
| B. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| C. | NA个氧气分子与NA个氖气分子的质量比是8:5 | |
| D. | 标准状况下,11.2 L CO2与常温常压下8.5 g NH3所含分子数相等 |
20.一定温度下,取pH=12的NaOH溶液和氨水各10mL,分别用蒸馏水冲稀至1L.关于稀释后的溶液的pH的说法正确的是( )
| A. | NaOH溶液的pH小于氨水的pH | B. | NaOH溶液的pH大于氨水的pH | ||
| C. | 两溶液的pH相等 | D. | 无法判别两溶液pH的相对大小 |
10.下列对于硝酸的认识,不正确的是( )
| A. | 浓硝酸在见光或受热时会发生分解 | B. | 金属与硝酸反应不产生氢气 | ||
| C. | 可用铁和铝制品盛装浓硝酸 | D. | 铜与硝酸的反应属于置换反应 |
17.下列物质都含有羟基(-OH),各羟基中氢原子的活性大小比较正确的是( )
①H2O ②H2SO4(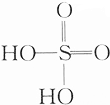 ) ③C2H5OH ④CH3COOH.
) ③C2H5OH ④CH3COOH.
①H2O ②H2SO4(
 ) ③C2H5OH ④CH3COOH.
) ③C2H5OH ④CH3COOH.| A. | ①>②>③>④ | B. | ②>③>④>① | C. | ②>④>①>③ | D. | ④>③>②>① |
12.在一定条件下,反应CO+NO2?CO2+NO△H=a kJ/mol达到平衡后,降低温度,混和气体的颜色变浅.下列判断正确的是( )
| A. | a<0 | |
| B. | 使用催化剂能加快反应速率并提高反应物的平衡转化率 | |
| C. | 降低温度,CO的平衡转化率降低 | |
| D. | 降低温度,各物质的浓度不变 |
13.下列有关实验的处理方法中,正确的是( )
| A. | 皮肤上沾了少量苯酚,先用稀NaOH溶液洗,再用水冲洗 | |
| B. | 做完银镜反应的试管,应该用稀硫酸清洗 | |
| C. | 试管中残留的苯酚,先用稀NaOH溶液洗,再用水冲洗 | |
| D. | 粘有酚醛树脂的试管,可先用水浸泡几分钟,软化,再清洗 |
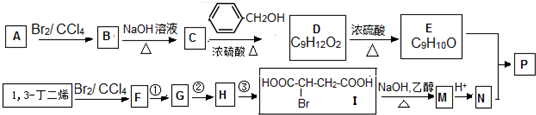
 ;
; . 高聚物P的亲水性比由E形成的聚合物的亲水性强(填“强”或“弱”).
. 高聚物P的亲水性比由E形成的聚合物的亲水性强(填“强”或“弱”). .
.