题目内容
下列说法中正确的是( )
| A、H2的摩尔质量是2g |
| B、H2的摩尔质量是2g/mol |
| C、H2的质量是2g |
| D、1摩尔H2的质量是2g/mol |
考点:摩尔质量
专题:阿伏加德罗常数和阿伏加德罗定律
分析:注意摩尔质量的单位为g/mol,质量的单位为g.
解答:
解:A、H2的摩尔质量是2g/mol,故A错误;
B、H2的摩尔质量是2g/mol,故B正确;
C、H2的质量不确定,需要给出物质的量等条件才可计算氢气的质量,故C错误;
D、1摩尔H2的质量是2g,故D错误.
故选:B.
B、H2的摩尔质量是2g/mol,故B正确;
C、H2的质量不确定,需要给出物质的量等条件才可计算氢气的质量,故C错误;
D、1摩尔H2的质量是2g,故D错误.
故选:B.
点评:本题考查了质量和摩尔质量的概念和单位问题,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
氧离子的结构示意图是( )
A、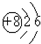 |
B、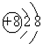 |
C、 |
D、 |
下列叙述正确的是( )
| A、1.00 molNaCl中含有6.02×1023个NaCl分子 |
| B、1.00molNaCl中,所有Na+的电子总数为8×6.02×1023 |
| C、电解58.5g 熔融的NaCl,能产生11.2L氯气(标准状况)、23.0g金属钠 |
| D、欲配置1.00L 1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水 |
用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、0.1mol/L100mL稀硫酸中含有硫酸根个数为0.1NA |
| B、1molCH3+(碳正离子)中含有电子数为10 NA |
| C、金属镁与足量的盐酸反应,转移电子数为2 NA时,生成氢气为22.4L |
| D、12.4g白磷中含有磷原子数为0.4NA |
下列有关物质的量的说法中正确的是( )
| A、物质的量就是物质的质量 |
| B、摩尔是国际单位制的七个基本物理量之一 |
| C、H2O的摩尔质量为18g |
| D、阿伏加德罗常数的数值约为6.02×1023 |
下列有关摩尔使用的说法中不正确的是( )
| A、1摩尔氧原子 |
| B、1摩尔氧分子 |
| C、1摩尔氧气 |
| D、1摩尔氧 |
互为同素异形体的一组物质是( )
| A、16 8O和18 8O |
| B、O2和O3 |
| C、CH≡CH和CH2=CH2 |
D、CH3CH2CH2CH3和 |
NO与NO2的混合气体60ml,通入水中,最后收集到的气体体积为40ml(气体体积均在相同条件下测定),则原混合气体中NO与NO2的体积比为( )
| A、1:2 | B、2:3 |
| C、3:2 | D、1:1 |