题目内容
2.下表中的实线表示元素周期表的部分边界.①-⑥分别表示元素周期表中对应位置的元素.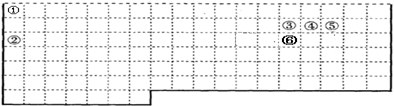
(1)请在上表中用实现补全元素周期表边界.
(2)写出①、③两种元素组成的正四面体化合物的电子式
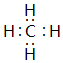 ,上述元素中,能和⑤号元素形成正四面体空间网状结构的化合物的化学式是SiO2.
,上述元素中,能和⑤号元素形成正四面体空间网状结构的化合物的化学式是SiO2.(3)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的产物是NH4NO3(写化学式),该物质含有的化学键是离子键、共价键.
(4)①和②元素在适当条件下能形成离子化合物,写出该化合物中所含阴、阳离子的结构示意图
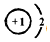 、
、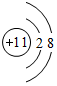 .
.
分析 由元素在周期表中的位置可知:①为H,②为Na,③为C,④为N,⑤为O,⑥为Si.
(1)第一周期含有2种元素,分别处于第1列、第18列,第二、第三周期中3~12列没有元素;
(2)①、③两种元素组成的正四面体化合物为CH4,上述元素中,能和⑤号元素形成正四面体空间网状结构的化合物二氧化硅;
(3)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的产物是硝酸铵;
(4)①和②元素在适当条件下能形成离子化合物为NaH.
解答 解:由元素在周期表中的位置可知:①为H,②为Na,③为C,④为N,⑤为O,⑥为Si.
(1)第一周期含有2种元素,分别处于第1列、第18列,第二、第三周期中3~12列没有元素,补全元素周期表边界为: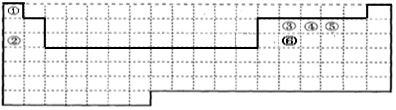 ,
,
故答案为: ;
;
(2)①、③两种元素组成的正四面体化合物为CH4,其电子式为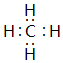 ,上述元素中,能和⑤号元素形成正四面体空间网状结构的化合物二氧化硅,
,上述元素中,能和⑤号元素形成正四面体空间网状结构的化合物二氧化硅,
故答案为: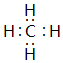 ;SiO2;
;SiO2;
(3)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的产物是NH4NO3,含有离子键、共价键,
故答案为:NH4NO3;离子键、共价键;
(4)①和②元素在适当条件下能形成离子化合物为NaH,H-离子结构示意图为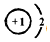 ,Na+离子结构示意图为
,Na+离子结构示意图为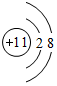 ,
,
故答案为: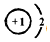 、
、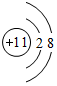 .
.
点评 本题考查元素周期表、常用化学用语、元素化合物知识,识记中学常见物质结构特点,金属氢化物在中学基本不涉及,但在试题中经常考查,需要学生注意理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是( )
①氯气 ②液氯 ③新制氯水 ④氯气的四氯化碳溶液 ⑤盐酸 ⑥盐酸与少量漂白粉的混合溶液.
①氯气 ②液氯 ③新制氯水 ④氯气的四氯化碳溶液 ⑤盐酸 ⑥盐酸与少量漂白粉的混合溶液.
| A. | ①②③ | B. | ①②③⑥ | C. | ③⑥ | D. | ③④⑥ |
13.保护环境已成为人类的共识,下列做法不利于环境保护的是( )
| A. | 火力发电厂的煤经粉碎、脱硫处理 | B. | 电镀废液经中和后直接排入到农田 | ||
| C. | 聚乳酸塑料代替传统塑料作购物袋 | D. | 回收并合理处理聚氯乙烯塑料废物 |
10.下列关于阿伏加德罗常数的说法正确的是( )
| A. | 阿伏加德罗常数是12 g碳中所含的碳原子数 | |
| B. | 24 g镁的原子最外层电子数为NA | |
| C. | 阿伏加德罗常数约是6.02×1023 | |
| D. | 阿伏加德罗常数的符号为NA,近似为6.02×1023 mol-1 |
17.已知0.3mol C在0.2mol O2中燃烧,至反应物耗尽,并放出X kJ热量.已知单质碳的燃烧热为Y kJ/mol,则1mol C与O2反应生成CO的反应热△H为( )
| A. | -Y kJ/mol | B. | -(5X-0.5Y)kJ/mol | C. | -(10X-Y)kJ/mol | D. | +(10X-Y)kJ/mol |
7.在相同温度时,100mL 0.01mol/L的醋酸溶液与10mL 0.1mol/L的醋酸溶液相比较,下列数值前者大于后者的是( )
| A. | 中和时所需NaOH的量 | B. | 电离的程度 | ||
| C. | H+的物质的量浓度 | D. | H+的物质的量 |
11.根据如图的溶解度曲线判断,下列说法错误的是( )
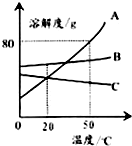

| A. | 50℃时A物质的溶解度最大 | |
| B. | 升温可使C物质的不饱和溶液变成饱和溶液 | |
| C. | 50℃时把90gA物质放入100g水中能得到190g溶液 | |
| D. | 将50℃三种物质的饱和溶液分别降温到20℃时,B溶液溶质质量分数最大 |
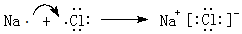 .
.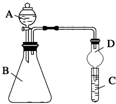 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.