题目内容
7.高中化学学习过程中的物质颜色是需要注意的.下列关于颜色的描述正确的个数是①氯水放久了会逐渐由黄绿色变成几乎无色
②AgBr见光分解会生成浅黄色的银
③KI溶液中加入淀粉溶液会变成紫色
④碘水中加入CCl4振荡静置后,CCl4层紫红色
⑤氢气能在氯气中燃烧,火焰为黄色( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
分析 ①新制氯水中:Cl2+H2O?HCl+HClO,氯水放久了因2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,溶解的Cl2逐渐全部反应最终变成稀盐酸;
②AgBr见光分解:2AgBr$\frac{\underline{\;光照\;}}{\;}$2Ag+Br2;
③根据能使淀粉溶液变成蓝色的是单质碘;
④碘水中加入CCl4振荡静置后,碘从水中转移到CCl4中,CCl4因溶解碘呈紫红色;
⑤氢气在氯气中燃烧发出苍白色火焰.
解答 解:①因新制氯水中:Cl2+H2O?HCl+HClO,氯水放久了因2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,溶解的Cl2逐渐全部反应最终变成稀盐酸,盐酸为无色,故①正确;
②因AgBr见光分解:2AgBr$\frac{\underline{\;光照\;}}{\;}$2Ag+Br2,Ag是黑色小颗粒,故②错误;
③因单质碘才能使淀粉溶液变成蓝色,KI溶液中I-不能使淀粉溶液变成蓝色,故③错误;
④碘水中加入CCl4振荡静置后,碘从水中转移到CCl4中,CCl4因溶解碘呈紫红色,故④正确;
⑤氢气在氯气中燃烧发出苍白色火焰,故⑤错误;
正确的是①④,
故选B.
点评 本题主要考查了一些常见物质的性质,掌握物质的性质是解题的关键,注意化学知识的积累,题目较简单.

练习册系列答案
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
12.下列有关说法不正确的是( )
| A. | 配制SnCl2溶液时,首先用盐酸酸化蒸馏水,然后加入SnCl2晶体 | |
| B. | 加热CH3COONa溶液(预先滴有少量酚酞),溶液颜色变深 | |
| C. | 常温下,Fe(NO3)3溶液中由水电离产生的[H+]等于10-10 mol•L-1 | |
| D. | NaHCO3作为发酵粉使用时,加入少量的明矾在水中能起到酸的作用 |
13.有KAl(SO4)2和K2SO4的混合溶液aL将它均分成两份,一份滴加BaCl2稀溶液,使SO42-离子完全沉淀,另一份滴加KOH溶液,使Al3+离子先沉淀后又恰好溶解,反应中消耗xmolBaCl2、ymolKOH,据此得知原混合溶液中的c(K+)/mol•L-1为( )
| A. | $\frac{4x-2y}{a}$ | B. | $\frac{2x-y}{a}$ | C. | $\frac{8x-3y}{2a}$ | D. | $\frac{8x-3y}{a}$ |
12.已知:pKa=-lgKa,25℃时,H2SO3的 pKa1=1.85,pKa2=7.19.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SO3溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法正确的是( )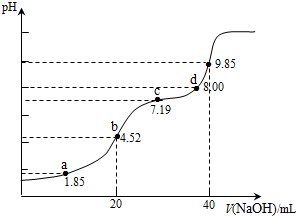

| A. | a点所得溶液中:2c(H2SO3)+c(SO32-)=0.1 mol•L-1 | |
| B. | b点所得溶液中:c(H2SO3)+c(H+)=c(SO32-)+c(OH-) | |
| C. | c点所得溶液中:c(Na+)<3c($HS{{{O}_{3}}^{-}}_{\;}$) | |
| D. | d点所得溶液中:c(Na+)>c(SO32-)>c(HSO3-) |
19.两种气态烃以任意比例混合,在105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L.下列各组混合烃中不符合此条件的是( )
| A. | CH4 C2H4 | B. | CH4 C3H4 | C. | C2H4 C3H4 | D. | C2H2 C3H6 |
17.2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM 2.5监测指标(PM 2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物).下列情况不会增加空气中PM 2.5的是( )
| A. | 直接露天焚烧秸秆 | B. | ?风能发电 | ||
| C. | 汽车直接排放尾气 | D. | 用石油作燃料 |
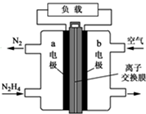 肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景.其工作原理如上图所示,回答下列问题:
肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景.其工作原理如上图所示,回答下列问题: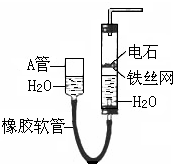 如图中的实验装置可用于制取乙炔.请填空:
如图中的实验装置可用于制取乙炔.请填空: .
.