题目内容
12.一粗硅,含杂质铁,取等质量的样品分别投入足量的稀盐酸和足量的稀氢氧化钠溶液中,放出等量的H2,则该粗硅中铁和硅的关系正确的是(提示:Si+2NaOH+H2O=Na2SiO3+2H2↑)( )| A. | 物质的量之比为1:1 | B. | 质量之比为4:1 | ||
| C. | 物质的量之比为l:2 | D. | 质量之比为2:1 |
分析 只有硅和NaOH溶液反应生成氢气,铁与HCl反应生成氢气,根据生成氢气的量计算粗硅中铁和硅的物质的量之比.
解答 解:根据电子得失:可知铁与盐酸反应:Fe~~H2,而硅与氢氧化钠反应:Si~~2H2,放出等量的H2,设生成氢的量为2mol,所以粗硅中铁和硅的物质的是之比为2:1,质量之比为2×56:1×28=4:1,
故选B.
点评 本题考查混合物反应的计算,侧重考查学生分析、计算能力,明确只有Si和NaOH溶液反应是解本题关键,利用关系式解答即可,题目难度不大.

练习册系列答案
相关题目
2.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.2mol/LCaCl2溶液中含Cl-数为0.4NA | |
| B. | 标准状况下,1.12L H2S气体分子中含0.5NA个质子 | |
| C. | 常温常压下,23 g NO2和N2O4的混合气体一定含有NA个氧原子 | |
| D. | 标准状况下,4.48L的水中含有H2O分子的数目为0.2NA |
3.25℃时,下列溶液中各离子的浓度关系不正确的是( )
| A. | 等体积、等浓度的K2CO3溶液与盐酸混合,则混合液中:c(K+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+) | |
| B. | 向氨水中滴加盐酸至中性,则溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | |
| C. | 等体积、等浓度的CH3COOH溶液与NaOH溶液混合后,溶液的pH=8,则c(OH-)-c(CH3COOH)=1×10-8mol•L-1 | |
| D. | 等体积、等浓度①NaCl、②CH3COONa、③NaClO溶液中离子总数大小顺序:③>②>① |
20.关于下列各装置图的叙述不正确的是( )
| A. | 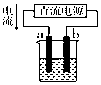 用装置精炼铜,则b极为精铜,电解质溶液为CuSO4溶液 | |
| B. | 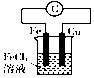 装置的总反应是Cu+2Fe3+=Cu2++2Fe2+ | |
| C. | 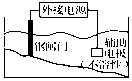 装置中钢闸门应与外接电源的负极相连 | |
| D. | 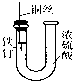 装置中的铁钉浸入浓硫酸中几乎没被腐蚀 |
7.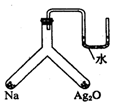 充分加热如图所示的密闭容器中放置有试剂的两个位置,若钠与氧化银均友应完且恢复到原来的温度时,U形管左右两侧液面相平,下列有关说法错误的是( )
充分加热如图所示的密闭容器中放置有试剂的两个位置,若钠与氧化银均友应完且恢复到原来的温度时,U形管左右两侧液面相平,下列有关说法错误的是( )
 充分加热如图所示的密闭容器中放置有试剂的两个位置,若钠与氧化银均友应完且恢复到原来的温度时,U形管左右两侧液面相平,下列有关说法错误的是( )
充分加热如图所示的密闭容器中放置有试剂的两个位置,若钠与氧化银均友应完且恢复到原来的温度时,U形管左右两侧液面相平,下列有关说法错误的是( )| A. | 装置内空气成分保持不变 | B. | 热稳定性:钠的氧化物强于Ag2O | ||
| C. | 装置内钠与Ag2O物质的量比为2:1 | D. | 有淡黄色固体生成 |
4.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | pH=2的HA溶液与pH=12的MOH碱溶液以任意比混合:c(H+)+c(M+)═c(OH-)+c(A-) | |
| B. | 0.1mol•L-1Na2SO3溶液:c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) | |
| C. | 等浓度、等体积的Na2CO3和NaHCO3混合溶液:$\frac{c{(HCO}_{3}^{-})}{c({H}_{2}C{O}_{3})}>$$\frac{c{(CO}_{3}^{2-})}{c{(HCO}_{3}^{-})}$ | |
| D. | 0.1mol•L-1CH3COONa溶液与0.1mol•L-1CaCl2溶液等体积混合:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(CL-) |