题目内容
11.下列说法不正确的是( )| A. | 比较去锈的铁钉和去锈的绕有细铜丝的铁钉与同浓度的盐酸反应速率快慢时,可以加K3[Fe(CN)6]沉淀,观察铁钉周围出现蓝色沉淀的快慢 | |
| B. | 探究温度对化学反应速率影响时,先将硫代硫酸钠与硫酸两种溶液混合后再用水浴加热 | |
| C. | 欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(试纸)为:中和滴定实验、pH试纸 | |
| D. | 从海带中提取碘,可将灰化后的海带加入水中煮沸一段时间后过滤,向滤液中滴入几滴硫酸,再加入适量H2O2溶液氧化,最后加入CCl4萃取分离 |
分析 A.亚铁离子和铁氰化钾溶液反应生成蓝色沉淀;
B.控制其他量相同,只控制温度不同;
C.确定醋酸的电离常数,根据CH3COOH?CH3COO-+H+,应分别确定CH3COOH的物质的量浓度和H+的物质的量浓度,可用滴定法确定CH3COOH的物质的量浓度,用pH试纸可粗略确定H+的物质的量浓度;
D.海带中含有碘离子,在酸性环境中过氧化氢能够氧化碘离子,碘单质易溶于有机溶剂.
解答 解:A.去锈的绕有细铜丝的铁钉在盐酸溶液中形成原电池,产生亚铁离子速度快,与铁氰化钾溶液反应生成蓝色沉淀所用的时间短,故A正确;
B.探究温度对反应速率的影响时,控制其他量相同,只控制温度不同,则应将混合物分别在热水、冷水中反应,故B错误;
C.可用滴定法确定CH3COOH的物质的量浓度,用pH试纸可粗略确定H+的物质的量浓度,进而计算电离常数,故C正确;
D.海带中含有碘离子,在酸性环境中过氧化氢能够氧化碘离子,碘单质易溶于CCl4,最后加入CCl4萃取分离,故D正确;
故选B.
点评 本题考查了物质性质和离子检验的实验操作,为高频考点,把握物质的性质及反应原理为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度中等.

练习册系列答案
相关题目
6.某实验小组对影响铝与盐酸反应的快慢的因素进行探究.下表是实验记录的数据.
(1)写出铝与盐酸反应的离子方程式:2Al+6H+=2Al3++3H2↑;
(2)实验①与实验②探究浓度对反应速率的影响,实验②与实验③探究温度对反应速率的影响.请将表中空白处填写完整,由实验得出的结论是:其他条件不变时,反应物浓度越大,反应速率越快,反应温度越高,反应速率越快.
(3)若实验④盐酸浓度为0.4mol/L,反应温度为40℃,铝片消失的时间大约为6.25s.实验⑤盐酸浓度为0.2mol/L,温度为50℃,铝片消失的时间与实验④相比可能更短的是⑤(填编号)
| 实验编号 | 盐酸的浓度 | 反应温度 | 铝片消失的时间 |
| ① | 0.1mol/L | 20℃ | 400s |
| ② | 0.2mol/L | 20℃ | 200s |
| ③ | 0.2mol/L | 30℃ | 50s |
(2)实验①与实验②探究浓度对反应速率的影响,实验②与实验③探究温度对反应速率的影响.请将表中空白处填写完整,由实验得出的结论是:其他条件不变时,反应物浓度越大,反应速率越快,反应温度越高,反应速率越快.
(3)若实验④盐酸浓度为0.4mol/L,反应温度为40℃,铝片消失的时间大约为6.25s.实验⑤盐酸浓度为0.2mol/L,温度为50℃,铝片消失的时间与实验④相比可能更短的是⑤(填编号)
16.表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素其原子结构示意图为 .
.
(2)表中能形成两性氢氧化物的元素其单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O=2KAlO2+3H2↑.
(3)④元素与⑦元素形成化合物的电子式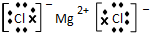 .
.
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4(填化学式).
(5)在⑨与④的单质中,化学性质较活泼的是K,①、②的气态氢化物中,比较稳定的是NH3(填化学式).
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)表中能形成两性氢氧化物的元素其单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O=2KAlO2+3H2↑.
(3)④元素与⑦元素形成化合物的电子式
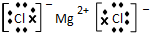 .
.(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4(填化学式).
(5)在⑨与④的单质中,化学性质较活泼的是K,①、②的气态氢化物中,比较稳定的是NH3(填化学式).
20.卤素是最活泼的一族非金属,下列关于卤族元素的说法正确的是( )
| A. | 卤素元素原子最外层电子数都是7 | B. | 从氟到碘,卤素原子半径依次减小 | ||
| C. | 卤素元素单质均为气态 | D. | 从氟到碘,非金属性逐渐增强 |
1.下列物质中,既含有离子键,又含有非极性共价键的是( )
| A. | Na2O2 | B. | CaCl2 | C. | NaOH | D. | NH4Cl |
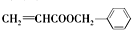 .
.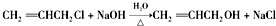 .
.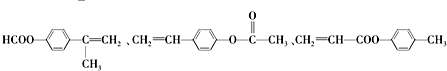 .
. .
.