题目内容
12.某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质.(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是B.
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)现有甲、乙、丙、丁四名同学进行Fe(OH)3胶体的制备
①甲同学的操作是:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mL FeCl3饱和溶液,用玻璃棒搅拌,继续煮沸至溶液呈红褐色,停止加热.请评价该操作是否正确正确.
②乙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确不正确.
(3)怎样检验制备的物质是否为胶体?利用丁达尔效应:让一束光线通过制得的Fe(OH)3胶体,从侧面观察到一条光亮的“通路”,说明已经制得胶体.
(4)取少量你制得的胶体加入试管中,加入(NH4)2SO4溶液,现象是产生红褐色沉淀,这种现象称为胶体的聚沉.
(5)氢氧化铁胶体稳定存在的主要原因是B.
A.胶粒直径小于1nm B.胶粒带正电荷C.胶粒作布朗运动 D.胶粒能透过滤纸.
分析 (1)实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液;
(2)制备氢氧化铁胶体时,不能用玻璃棒搅拌,防止胶体聚沉,当溶液变为红褐色时应立即停止加热,如继续加热会导致胶体聚沉;
(3)胶体具有丁达尔性质,是区别其它分散系的独特性质;
(4)胶体粒子带有电荷,加入电解质溶液消除粒子所带电荷,会是胶粒之间的排斥力减小,使胶体聚沉;
(5)胶粒带正电荷,相互排斥,而不易产生较大粒子而聚沉.
解答 解:(1)实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热,故答案为:B;
(2)①在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热,这是制备氢氧化铁胶体的正确操作,正确,故答案为:正确;
②加热到继续沸腾,不能继续加热,错误,故答案为:不正确;
(3)胶体具有丁达尔效应,当用激光笔照射时,会有一道明亮的光路,是区别其它分散系的独特性质,当让一束光线通过制得的Fe(OH)3胶体,从侧面观察到一条光亮的“通路”,说明已经制得胶体,
故答案为:利用丁达尔效应:让一束光线通过制得的Fe(OH)3胶体,从侧面观察到一条光亮的“通路”,说明已经制得胶体;
(4)胶体粒子带有电荷,加入电解质溶液消除粒子所带电荷,会使胶粒之间的排斥力减小,使胶体聚沉生成红褐色沉淀,
故答案为:产生红褐色沉淀;聚沉;
(5)胶体具有很强的吸附能力,能吸附溶液中的离子而带电荷,胶粒之间相互排斥,而不易产生较大微粒而聚沉,故答案为:B.
点评 本题考查胶体的制备、性质,题目难度不大,易错点为胶体的制备,本题重点把握胶体的制备.

练习册系列答案
相关题目
7.某溶液中含有0.005mol FeBr2及其他物质,向该溶液中通入134.4mL(标准状况)Cl2,溶液中只有FeBr2与Cl2反应,则通入Cl2后溶液中可能大量存在的离子是( )
| A. | Fe2+、Fe3+、Br-、NO3- | B. | Fe2+、H+、NO3-、K+ | ||
| C. | Fe3+、Br-、NO3-、Cl- | D. | Fe2+、Br-、NO3-、Cl- |
3.某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g)?2C(g),达到平衡后,其他条件不变时,若改变影响平衡的一个条件,测得容器中物质的浓度、反应速率随时间的变化如图所示.下列说法中正确是:( )


| A. | 30min时降低温度,40min时升高温度 | |
| B. | 前8min A的平均反应速率为0.17mol/(L•min) | |
| C. | 反应方程式中的x=1,正反应为吸热反应 | |
| D. | 20min~40min间该反应的平衡常数均为4 |
17.下列变化中,需要加入氧化剂才能实现的是( )
| A. | CO→CO2 | B. | MnO4→Mn2+ | C. | SO2→H2SO3 | D. | NaCl→AgCl |
1.下列关于物质的量浓度表述正确的是( )
| A. | 0.3 mol•L-1 Na2SO4溶液中含有Na+和SO${\;}_{4}^{2-}$总物质的量为0.9 mol | |
| B. | 50mL 1 mol•L-1的KCl溶液和100mL 0.5 mol•L-1MgCl2溶液中,Cl-的物质的量浓度相等 | |
| C. | 用1 L水吸收22.4 L氨气所得氨水的浓度是1 mol•L-1 | |
| D. | 10℃时0.35 mol•L-1的KCl饱和溶液100 mL,蒸发掉5 g水,再冷却到10℃时,它的物质的量浓度仍为0.35 mol•L-1 |
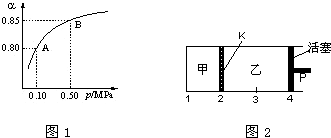

 某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图:
某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图: