题目内容
现有四种短周期元素X、Y、Z、W,它们的原子序数依次增大.其中:①X原子是元素周期表中原子半径最小的;②Y的L层电子是K层电子的2倍;③Z的最外层电子是内层电子的3倍;④W与X同主族.请回答下列问题:
(1)X的元素符号为 ,Y在周期表中的位置是 ,Z单质的化学式为 .
(2)X与Z组成的含有非极性共价键的化合物的分子式为 ;化合物W2Z2的电子式为 .
(3)向Na2SiO3的溶液中缓慢通入过量的YZ2,反应的离子方程式是 ;分子中有10个电子,则X与Z组成的分子为 、X与Y组成的分子式为 .
(1)X的元素符号为
(2)X与Z组成的含有非极性共价键的化合物的分子式为
(3)向Na2SiO3的溶液中缓慢通入过量的YZ2,反应的离子方程式是
考点:位置结构性质的相互关系应用
专题:基本概念与基本理论
分析:短周期元素X、Y、Z、W的原子序数依次增大,X原子是元素周期表中原子半径最小的,则X为氢元素;Y的L层电子是K层电子的2倍,则Y为碳元素;Z的最外层电子是内层电子的3倍,则Z为氧元素;W与X同主族,原子序数比氧大的短周期元素,则W为钠元素,据此答题;
解答:
解:短周期元素X、Y、Z、W的原子序数依次增大,X原子是元素周期表中原子半径最小的,则X为氢元素;Y的L层电子是K层电子的2倍,则Y为碳元素;Z的最外层电子是内层电子的3倍,则Z为氧元素;W与X同主族,原子序数比氧大的短周期元素,则W为钠元素,
(1)X为氢元素,元素符号为H,Y为碳元素,在周期表中的位置是第二周期第ⅣA族,Z为氧元素,单质的化学式为 O2,故答案为:H;第二周期第ⅣA族;O2;
(2)X与Z组成的含有非极性共价键的化合物的分子式为 H2O2;化合物W2Z2为Na2O2,它的电子式为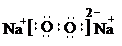 ,故答案为:H2O2;
,故答案为:H2O2;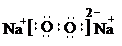 ;
;
(3)向Na2SiO3的溶液中缓慢通入过量的CO2,反应的离子方程式是2 CO2+2 H2O+SiO32-═2 HCO3-+H2SiO3↓;分子中有10个电子,则X与Z组成的分子为H2O、X与Y组成的分子式为CH4,故答案为:2 CO2+2 H2O+SiO32-═2 HCO3-+H2SiO3↓; H2O;CH4;
(1)X为氢元素,元素符号为H,Y为碳元素,在周期表中的位置是第二周期第ⅣA族,Z为氧元素,单质的化学式为 O2,故答案为:H;第二周期第ⅣA族;O2;
(2)X与Z组成的含有非极性共价键的化合物的分子式为 H2O2;化合物W2Z2为Na2O2,它的电子式为
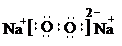 ,故答案为:H2O2;
,故答案为:H2O2;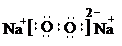 ;
;(3)向Na2SiO3的溶液中缓慢通入过量的CO2,反应的离子方程式是2 CO2+2 H2O+SiO32-═2 HCO3-+H2SiO3↓;分子中有10个电子,则X与Z组成的分子为H2O、X与Y组成的分子式为CH4,故答案为:2 CO2+2 H2O+SiO32-═2 HCO3-+H2SiO3↓; H2O;CH4;
点评:本题主要考查了元素周期表、电子式、离子反应等知识点,比较简单,解题时注意根据原子结构确定元素的种类.

练习册系列答案
相关题目
已知:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ?mol-12CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ?mol-1H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1下列说法正确的是( )
| A、H2(g)的燃烧热为571.6 kJ?mol-1 | ||||||
| B、同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 | ||||||
C、
| ||||||
| D、3H2(g)+CO2(g)=CH3OH(l)+H2O(l)△H=+135.9 kJ?mol-1 |
下列物质中的杂质(括号内)可用加热的方法除去的是( )
| A、CO2(CO) |
| B、NaHCO3(Na2CO3) |
| C、Na2CO3(NaHCO3) |
| D、NaOH(NaHCO3) |
在实验室从自来水制取蒸馏水的实验中,下列说法错误的是( )
| A、蒸馏烧瓶中要放入碎瓷片防止暴沸 |
| B、温度计的水银球放在支管口稍下位置,不能插入液面 |
| C、冷凝水应该是下进上出,与蒸汽的流向相反 |
| D、开始蒸馏时,应该先加热,再开冷凝水;蒸馏完毕,应该先关冷凝水再撤酒精灯 |
下列仪器使用时不允许用酒精灯加热的是( )
| A、量筒 | B、蒸馏烧瓶 |
| C、试管 | D、烧杯 |
在强酸性无色透明的溶液中能够大量共存的离子组是( )
| A、Na+、Mg2+、NO3-、Cl- |
| B、Na+、K+、CO32-、NO3- |
| C、K+、Ba2+、HCO3-、Cl- |
| D、Na+、K+、MnO4-、SO42- |