题目内容
8.将10.7g 氯化铵固体与足量熟石灰混合加热,使之充分反应.(1)写出反应的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑
(2)生成的氨气在标准状况下的体积是4.48L.
(3)用氨可以把一氧化氮还原成氮气,反应的化学方程式为:4NH3 +6NO═5N2 +6H2O,此反应中氧化产物与还原产物的物质的量之比为2:3.
分析 (1)氯化铵与熟石灰反应生成氯化钙、水、氨气;
(2)n(NH4Cl)=$\frac{10.7g}{53.5g/mol}$=0.2mol,由N原子守恒可知,生成氨气为0.2mol;
(3)氨可以把一氧化氮还原成氮气,还生成水,只有N元素的化合价变化,以此来解答.
解答 解:(1)氯化铵固体与足量熟石灰混合加热,发生反应为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
(2)n(NH4Cl)=$\frac{10.7g}{53.5g/mol}$=0.2mol,由N原子守恒可知,生成氨气为0.2mol,其标准状况下体积为0.2mol×22.4L/mol=4.48L,
故答案为:4.48;
(3)氨可以把一氧化氮还原成氮气,反应的化学方程式为4NH3 +6NO═5N2 +6H2O,由N元素的化合价变化可知,4molN失去电子等于6molN得到电子,氧化产物与还原产物均为氮气,此反应中氧化产物与还原产物的物质的量之比为2:3,
故答案为:4NH3 +6NO═5N2 +6H2O;2:3.
点评 本题考查化学反应的计算,为高频考点,把握发生的反应、物质的量计算、反应中元素的化合价变化为解答的关键,侧重分析与计算能力的考查,注意原子守恒的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.某兴趣小组设计并进行了以下实验来探究Cl2、漂白粉的制备及有关性质.
(1)实验室拟用下列装置制备干燥纯净的氯气,请按照气体从左向右流动的方向将仪器进行连接:H→A、B→C、D→E:广口瓶Ⅱ中的试剂为饱和食盐水.
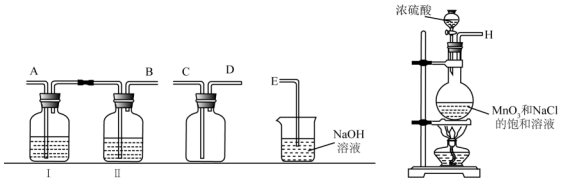
(2)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(3)某学生设计如下实验进一步探究SO2与漂粉精的反应:
①pH试纸颜色的变化说明漂粉精溶液具有的性质是碱性、漂白性.
②该同学推测现象i的雾状物由盐酸小液滴形成,进行如下实验加以进一步验证:
a.用湿润的碘化钾淀粉试纸检验雾状物;
b.搜集雾状物,用酸化的AgNO3溶液检验,产生白色沉淀.
实验a的目的是排除氯气干扰
③推测ii中溶液变为黄绿色,是由于产生了Cl2(写化学式),iii中产生的大量白色沉淀应为CaSO4(写化学式)
(1)实验室拟用下列装置制备干燥纯净的氯气,请按照气体从左向右流动的方向将仪器进行连接:H→A、B→C、D→E:广口瓶Ⅱ中的试剂为饱和食盐水.

(2)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(3)某学生设计如下实验进一步探究SO2与漂粉精的反应:
| 操作 | 现象 |
| 取漂粉精固体,加入水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的PH | 试纸先变蓝(约为12),后褪色 |
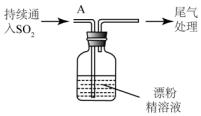 | i.液面上方出现雾状物 ii.稍后,出现浑浊,溶液变为黄绿色 iii.稍后,产生大量白色沉淀,黄绿色褪去 |
②该同学推测现象i的雾状物由盐酸小液滴形成,进行如下实验加以进一步验证:
a.用湿润的碘化钾淀粉试纸检验雾状物;
b.搜集雾状物,用酸化的AgNO3溶液检验,产生白色沉淀.
实验a的目的是排除氯气干扰
③推测ii中溶液变为黄绿色,是由于产生了Cl2(写化学式),iii中产生的大量白色沉淀应为CaSO4(写化学式)
13.下列有关说法正确的是( )
| A. | 实验室制氢气,为了加快反应速率,可向稀硫酸中滴加少量硝酸铜溶液 | |
| B. | 可用勒夏特列原理解释2NO2(g)?N2O4(g)体系加压后颜色变深 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0可通过加压方式增大其平衡常数 | |
| D. | 二氧化硫和乙烯两种气体分别通入Br2的CCl4溶液,能使溶液褪色的是乙烯气体 |
20.下列物质不属于合金的是( )
| A. | 金刚石 | B. | 硬铝 | C. | 不锈钢 | D. | 青铜 |
17.可检验FeC13溶液中是否含FeCl2的试剂是( )
| A. | KSCN溶液 | B. | 氯水 | C. | NaOH溶液 | D. | 酸性KMnO4溶液 |
18.下列说法正确的是( )
| A. | 蔬菜水果多属于碱性食物,对人体健康有益 | |
| B. | 棉花、合成橡胶都属于合成材料 | |
| C. | 蚕丝、羊毛完全燃烧只生成CO2和H2O | |
| D. | 苯、植物油均能使酸性KMnO4溶液褪色 |
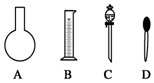 实验需要0.80mol•L-1 NaOH溶液475mL和0.40mol•L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
实验需要0.80mol•L-1 NaOH溶液475mL和0.40mol•L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题: