题目内容
19.某研究小组在实验室用重晶石(主要成分为BaSO4)对工业过程进行模拟实验,其焙烧过程的主要反应如下:BaSO4(s)+4C(s)$\stackrel{高温}{?}$4CO(g)+BaS(s)
(1)高温焙烧所产生的气体必须处理,其装置为D.

(2)重晶石高温焙烧产生的固体在用盐酸溶解时所产生的气体必须用CuSO4溶液吸收,写出吸收反应的化学方程式为H2S+CuSO4=CuS↓+H2SO4.
(3)在实验室进行过滤操作时所使用的玻璃仪器除了烧杯外,还有漏斗、玻璃棒.
(4)无论在工业上还是在实验室里,从滤液中获得目标产物BaCl2,采用的方法一般都是加热蒸发、冷却结晶、过滤
、洗涤、干燥,而不是直接将溶液蒸干,其理由是直接蒸干溶液将把溶液中一切离子均变成固体,引入杂质.
(5)在实验室里BaCl2常用于检验溶液中是否存在SO42-离子.为了避免Ag+、CO32-、SO32-等阴、阳离子的干扰,可先向溶液中加入盐酸.
分析 (1)根据反应BaSO4(s)+4C(s)$\stackrel{高温}{?}$4CO(g)+BaS(s)可知,高温焙烧所产生的气体为CO,有毒,会污染空气,要经点燃处理;
(2)重晶石高温焙烧产生的固体在用盐酸溶解时所产生的气体为H2S,H2S与CuSO4溶液反应生成硫化铜沉淀和水;
(3)过滤操作时所使用的玻璃仪器除了烧杯外,还有漏斗和玻璃棒;
(4)无论在工业上还是在实验室里,从滤液中获得目标产物BaCl2,因溶液中有其它可溶的杂质离子,所以采用的方法一般都是加热蒸发、冷却结晶、过滤、洗涤、干燥,而不是直接将溶液蒸干,以防止其它杂质也留在BaCl2中;
(5)在实验室里BaCl2常用于检验溶液中是否存在SO42-离子,要先加入过量的盐酸,可以避免Ag+、CO32-、SO32-等阴、阳离子的干扰,据此答题.
解答 解:(1)根据反应BaSO4(s)+4C(s)$\stackrel{高温}{?}$4CO(g)+BaS(s)可知,高温焙烧所产生的气体为CO,有毒,会污染空气,要经点燃处理,故选D;
(2)重晶石高温焙烧产生的固体在用盐酸溶解时所产生的气体为H2S,H2S与CuSO4溶液反应生成硫化铜沉淀和水,反应方程式为H2S+CuSO4=CuS↓+H2SO4,
故答案为:H2S+CuSO4=CuS↓+H2SO4;
(3)过滤操作时所使用的玻璃仪器除了烧杯外,还有漏斗和玻璃棒,
故答案为:漏斗、玻璃棒;
(4)无论在工业上还是在实验室里,从滤液中获得目标产物BaCl2,因溶液中有其它可溶的杂质离子,所以采用的方法一般都是加热蒸发、冷却结晶、过滤、洗涤、干燥,而不是直接将溶液蒸干,以防止其它杂质也留在BaCl2中,
故答案为:冷却结晶、过滤;直接蒸干溶液将把溶液中一切离子均变成固体,引入杂质;
(5)在实验室里BaCl2常用于检验溶液中是否存在SO42-离子,要先加入过量的盐酸,可以避免Ag+、CO32-、SO32-等阴、阳离子的干扰,
故答案为:盐酸.
点评 本题考查较为综合,题目具有一定难度,涉及实验基本操作、物质的提纯、离子的检验等问题,解题时注意基础知识的灵活运用;

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案| A. | 裂化可以提高汽油等轻质油的产量和质量 | |
| B. | 硬脂酸甘油酯皂化反应后得到的主要产品是硬脂酸和甘油 | |
| C. | 乙醇、乙酸、乙酸乙酯分子中均存在-OH | |
| D. | 向2mL苯中加入1mL碘的CCl4溶液,振荡后静置,上层呈紫色 |
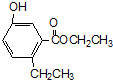
| A. | R分子中有7种化学环境均不同的氢原子 | |
| B. | R和溴水反应后所得产物的化学式为C11H12O3Br2 | |
| C. | R在碱性条件下的水解产物均难溶于水 | |
| D. | R不能使酸性高锰酸钾溶液褪色 |
 甲烷分子中的4个氢原子都可以被取代.若甲烷分子中的4个氢原子被苯基取代,则可得到的分子如图所示,对该分子的描述中,不正确的是( )
甲烷分子中的4个氢原子都可以被取代.若甲烷分子中的4个氢原子被苯基取代,则可得到的分子如图所示,对该分子的描述中,不正确的是( )| A. | 化学式为C25H20 | B. | 此物质属芳香烃类物质 | ||
| C. | 所有碳原子都在同一平面上 | D. | 最多有13个碳原子在同一平面上 |
| A. | 10:1 | B. | 1:10 | C. | 1:100 | D. | 1:2 |
| A. | 将250 g CuSO4•5H2O溶解在1 L水中 | |
| B. | 将22.4 L HCl气体溶于水配成1 L溶液 | |
| C. | 将1 L 10 mol•L-1的浓盐酸加入9 L水中 | |
| D. | 将10 g NaOH溶解在少量水中,再加蒸馏水到溶液体积为250 mL |
| A. | Cl2 | B. | Ca(ClO)2 | C. | HClO | D. | HCl |
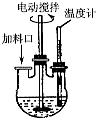 实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入.
实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入.