题目内容
19.关于CH4说法错误的是( )| A. | 固态时属于分子晶体 | B. | 正四面体结构的分子 | ||
| C. | 与CCl4结构相似、分子间存在氢键 | D. | 含极性键的非极性分子 |
分析 A.分子晶体是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体;
B.正四面体中,4个键的键长、键角都相等,一般只有同种元素构成的化学键才能完全相同,甲烷为正四面体结构,C原子位于正四面体的中心;
C.N、O、F元素的电负性较强,对应的氢化物可形成氢键,CH4与CCl4结构相似,但CCl4分子间不存在氢键;
D.同种元素原子间形成的共价键是非极性共价键,不同种元素原子之间形成的共价键是极性共价键;分子结构不对称,正负电荷的中心不重合的分子为极性分子,而结构对称且正负电荷的中心重合的分子为非极性分子,以此来解答.
解答 解:A.甲烷是碳原子和氢原子间通过共价单键形成的分子,其结构式为 ,属于分子晶体,由分子直接构成,故A正确;
,属于分子晶体,由分子直接构成,故A正确;
B.甲烷分子中碳原子位于正四面体中心上,四个顶点上分别含有一个氢原子,为正四面体结构,故B正确;
C.甲烷与CCl4结构相似,都为正四面体结构的分子,氢键是一种较强的分子间作用力,是由电负性强的原子(如F,O,N)对氢原子的吸引力产生的,CCl4无F,O,N元素,分子间不存在氢键,故C错误;
D.CH4含有C-H极性键,CH4空间构型为正四面体型,结构对称且正负电荷的中心重合,为非极性分子,故D正确;
故选C.
点评 本题考查甲烷结构有关知识,涉及分子空间构型、氢键、分子极性的判断,注意判断键的极性,分子极性的判断,抓住正负电荷的中心是否重合,题目难度不大,注意相关基础知识的积累.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
9.下列各组离子在给出条件下一定能大量共存的是( )
| A. | 在pH=1的溶液中:NH4+、K+、ClO-、Cl- | |
| B. | 水电离的c(H+)=1.0×10-13mol•L-1的溶液中:Na+、Mg2+、Ca2+、I- | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在c(H+)=1.0×10-13mol•L-1的溶液中:Na+、S2-、AlO2-、SO32- |
10.高温及一定催化剂作用下某反应达平衡,平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$,恒容时,温度升高,H2浓度减小.下列说法:正确的是( )
| A. | 平衡后向容器中再充入与初始投料相同物质的量的CO2和H2,则CO的平衡浓度变为原来的2倍 | |
| B. | 恒温恒容下,增大压强,H2的浓度一定减小 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 该反应化学方程式为:CO2(g)+H2(g)?CO(g)+H2O(g)△H<0 |
7.化学与环境、材料、信息、能源关系密切,下列说法错误的是( )
| A. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 | |
| B. | 硫酸铁易溶于水,可作净水剂 | |
| C. | 我国首艘航母“辽宁舰”上用于舰载机降落的拦阻索是特种钢缆,属于金属材料 | |
| D. | 减少烟花爆竹的燃放,有利于降低空气中的PM2.5含量 |
4.制取水处理剂C1O2(其部分性质如下表所示)的方法之一是利用草酸(H2C2O4)与氯酸钾反应,反应的化学方程式为2KC1O3+aH2C2O4+H2SO4=2C1O2↑+K2SO4+2CO2↑+bH2O.下列有关该反应的说法不正确的是( )
| 熔点/℃ | 沸点/℃ | 水溶性 |
| -59.5 | 11.0 | 极易溶解 |
| A. | 化学方程式中的a=l,b=2 | |
| B. | 草酸起到还原剂的作用 | |
| C. | KC1O3中只有Cl元素被还原 | |
| D. | 在标准状况下生成5.6L C1O2,转移0.2mol电子 |
4.常温下pH=3的CH3COOH溶液,下列叙述不正确的是( )
| A. | 与等体积pH=11的NaOH溶液混合后所得溶液显酸性 | |
| B. | c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 该溶液中由水电离出的c(H+)是1.0×10-11 mol/L | |
| D. | 加入少量CH3COONa固体后,c(CH3COO-)降低 |

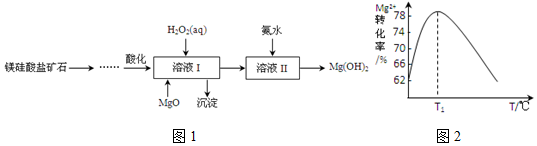
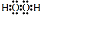 .溶液 I中加入H2O2溶液发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
.溶液 I中加入H2O2溶液发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.