题目内容
常温下,2L物质的量浓度为0.5mol?L-1 KOH溶液含有( )
| A、1 mol的K+ |
| B、0.5 mol的H+ |
| C、1.0 mol的H+ |
| D、1.0 mol的OH- |
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:根据n=cV计算KOH的物质的量,溶液中KOH完全电离n(K+)=n(KOH),溶液中OH-离子来源于KOH、水的电离,H+来源于水的电离,碱性条件下其浓度很小.
解答:
解:溶液中KOH的物质的量=2L×0.5mol/L=1mol,溶液中KOH完全电离,n(K+)=n(KOH)=1mol,KOH电离的OH-为1mol,溶液中OH-离子来源于KOH、水的电离,故n(OH-)>1mol,H+来源于水的电离,碱性条件下H+浓度很小,溶液中n(H+)远远小于1mol,
故选A.
故选A.
点评:本题考查物质的量浓度有关计算,难度中等,D选项为易错点,学生容易忽略水电离产生氢氧根离子.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、1mol Cl2通入含有2mol FeI2的溶液中:2Fe2++2I-+2Cl2═2Fe3++4Cl-+I2 |
| B、澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| C、AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O |
| D、向银氨溶液中加入足量的盐酸:[Ag(NH3)2]++OH-+3H+═Ag++2NH4++H2O |
下列关于2mol?L-1 NaOH 溶液的说法中,不正确的是( )
| A、将80 g NaOH 溶于1 L水中,所得溶液中NaOH的物质的量浓度为2 mol?L-1 |
| B、1 L溶液中含2 mol NaOH |
| C、溶液中含2 mol钠离子和2 mol氢氧根离子 |
| D、溶液中钠离子的浓度是2 mol?L-1 |
下列有关化学用语的说法中不正确的是( )
A、-OH与 都表示羟基 都表示羟基 |
B、聚丙烯的结构简式: |
C、CH4分子的球棍模型: |
D、次氯酸分子的电子式: |
下列化工生产过程中发生的反应,不属于氧化还原反应的是( )
| A、用氨气制硝酸 |
| B、用石灰石制生石灰 |
| C、用氯气制漂白粉 |
| D、从卤水中提取溴单质 |
在下列物质中,既具有氧化性又具有还原性的是( )
| A、铁 | B、硫 | C、铁和硫 | D、氢气 |


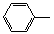 -CH=CH2)和D(HO-
-CH=CH2)和D(HO-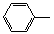 -CHO)按如下方法合成:
-CHO)按如下方法合成: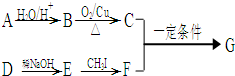
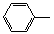 -ONa+RCH2I→
-ONa+RCH2I→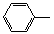 -OCH2R
-OCH2R