题目内容
19.能正确表示下列反应的离子方程式为( )| A. | 硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ | |
| B. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O | |
| C. | NaClO和NaOH的混合溶液中通入少量的SO2:ClO-+H2O+SO2=C1-+SO42-+2H+ | |
| D. | 大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
分析 A.硝酸具有强的氧化性,能够氧化二价铁离子和硫离子;
B.氢氧化钠过量,铵根离子、碳酸氢根离子都反应;
C.次氯酸根离子具有强的氧化性,能够氧化硫酸根离子;
D.二者反应生成醋酸钙、二氧化碳和水.
解答 解:A.硝酸具有氧化性,能氧化FeS,因此产物应该是硝酸铁、硫酸和一氧化氮,离子方程式:3FeS+18H++9NO3-=3Fe3++3H2SO4+9NO↑+6H2O,故A错误;
B.NH4HCO3溶于过量的NaOH溶液中,离子方程式:NH4++HCO3-+2OH-=CO32-+H2O+NH3•H2O,故B错误;
C.NaClO和NaOH的混合溶液中通入少量的SO2,离子方程式:2OH-+ClO-+H2O+SO2=C1-+SO42-+2H2O,故C错误;
D.大理石溶于醋酸中,离子方程式:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,侧重考查复分解反应、氧化还原反应的离子方程式书写,明确物质的性质及发生反应实质是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.关于下列四个图象的说法不正确的是( )
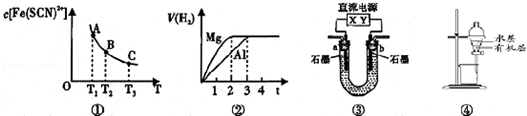

| A. | 已知图①是体系Fe3+(aq)+SCN-(aq)?Fe(SCN)2+(aq)中的c[Fe(SCN)2+]与温度T的平衡图象,A点与B点相比,A点的c(Fe3+)更小 | |
| B. | 图②表示镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积V 与时间t的关系.则反应中镁和铝的反应速率之比为2:3 | |
| C. | 图③直流电源Y极为正极,U形管中为AgNO3溶液,则b管中电极反应式是:4OH--4e-═O2↑+2H2O | |
| D. | 图④表示分离CCl4萃取碘水后已分层的有机层和水层 |
10.实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为:K=$\frac{c({H}_{2}C(CO))}{C({H}_{2}O)}$,它所对应的化学方程式为:C(s)+H2O(g)?CO(g)+H2(g)
(2)已知在400℃时,N2 (g)+3H2(g)?2NH3(g)△H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应V(N2)正=V(N2)逆(填:>、<、=、不能确定).
欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的正确措施是a(填序号)
a.缩小体积增大压强 b.升高温度 c.加催化剂 d.使氨气液化移走
(3)在一定体积的密闭容器中,进行如下化学反应:A(g)+3B(g)?2C(g)+D(s)△H,其化学平衡常数K与温度t的关系如下表:
请完成下列问题:
①判断该反应的△H>0(填“>”或“<”)
②在一定条件下,能判断该反应一定达化学平衡状态的是cd(填序号).
a.3v(B)(正)=2v(C)(逆)b.A和B的转化率相等
c.容器内压强保持不变 d.混合气体的密度保持不变.
(1)已知某反应的平衡表达式为:K=$\frac{c({H}_{2}C(CO))}{C({H}_{2}O)}$,它所对应的化学方程式为:C(s)+H2O(g)?CO(g)+H2(g)
(2)已知在400℃时,N2 (g)+3H2(g)?2NH3(g)△H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应V(N2)正=V(N2)逆(填:>、<、=、不能确定).
欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的正确措施是a(填序号)
a.缩小体积增大压强 b.升高温度 c.加催化剂 d.使氨气液化移走
(3)在一定体积的密闭容器中,进行如下化学反应:A(g)+3B(g)?2C(g)+D(s)△H,其化学平衡常数K与温度t的关系如下表:
| t/K | 300 | 400 | 500 | … |
| K/(mol•L-1)2 | 4×106 | 8×107 | K1 | … |
①判断该反应的△H>0(填“>”或“<”)
②在一定条件下,能判断该反应一定达化学平衡状态的是cd(填序号).
a.3v(B)(正)=2v(C)(逆)b.A和B的转化率相等
c.容器内压强保持不变 d.混合气体的密度保持不变.
7.对下列符号意义的表述正确的是( )
| A. | N2:两个氮原子 | B. | 2H:两个氢元素 | ||
| C. | 2H2O:两个水分子 | D. | Ca2+:钙元素的化合价为+2价 |
14.下列说法正确的是( )
| A. | 只含一种元素的物质一定是单质 | B. | 只含一种分子的物质一定纯净物 | ||
| C. | 非金属氧化物一定是酸性氧化物 | D. | 有单质生成的反应一定是置换反应 |
11.可逆反应mA(g)+nB(g)?xC(g)在不同温度及压强(p1和p2)条件下反应物A的转化率的变化情况如图所示.下列判断正确的是( )

| A. | 正反应吸热,m+n>x | B. | 正反应吸热,m+n<x | ||
| C. | 正反应放热,m+n<x | D. | 正反应放热,m+n>x |
8.我国“长征二号”火箭的主要燃料是偏二甲肼(用R表示),在火箭发射时,偏二甲肼与四氧化二氮剧烈反应,产生大量气体并释放出大量的热,该反应的化学方程式为:R+2N2O4═3N2+4H2O+2CO2,下列说法错误的是( )
| A. | 此反应是氧化还原反应 | |
| B. | N2O4在反应中作还原剂 | |
| C. | 反应瞬间产生大量高温气体,推动火箭飞行 | |
| D. | R的分子式为C2H8N2 |
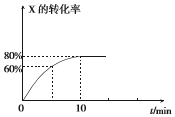 恒定温度为T1℃时,在容积为10L的密闭容器中充人1.0mol X和0.80mol Y,发生反应:
恒定温度为T1℃时,在容积为10L的密闭容器中充人1.0mol X和0.80mol Y,发生反应: