题目内容
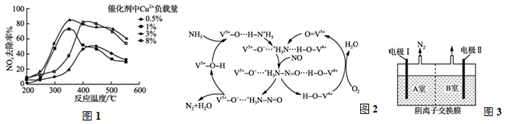
9.单质铁(Fe)可将水体中的硝酸盐(NO3-)转化为铵盐(NH4+)而去除掉,现将足量铁粉投入水体中,经24小时测定NO3-的去除率和初始pH的关系如图所示,已知pH=2.5时,在铁粉的外层包裹的主要是其氧化产物NO3-(可导电),而pH=4.5时,则是不导电的 FeO(OH),下列说法不正确的是( )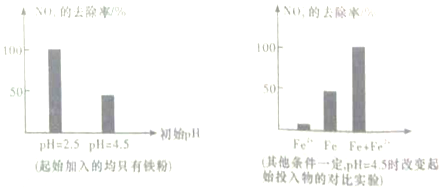
| A. | pH=4.5时,NO3-的去除率低,其原因可能是FeO(OH) 不导电,阻碍电子转移 | |
| B. | 通过对比试验发现,在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率,可能原因是Fe2+将NO3-直接还原了 | |
| C. | 加入Fe2+可能发生的反应是Fe2++2FeO(OH)═Fe3O4+2H+ | |
| D. | 由图猜测,溶液中H+浓度越大,对NO3-的去除率越高 |
分析 A.pH=4.5时,不导电的 FeO(OH)阻碍电子转移;
B.在初始pH=4.5的水体中补充一定量的Fe2+,NO3-的去除率并未提高;
C. FeO(OH)不导电,加入Fe2+可能与之发生氧化还原反应导电;
D.PH越小酸性越强.
解答 解:A.NO3-的去除是单质铁失去电子,硝酸盐(NO3-)中+5价的氮转化为铵盐(NH4+)中-3价的氮,存在电子转移,因pH=4.5时,不导电的 FeO(OH)阻碍电子转移,所以pH=4.5时,NO3-的去除率低,故A正确;
B.通过对比试验发现,在初始pH=4.5的水体中投入补充一定量的Fe2+,NO3-的去除率并未提高,同时加入足量的铁粉,提高NO3-的去除率,显然不是Fe2+将NO3-直接还原了,故B错误;
C.单质铁(Fe)可将水体中的硝酸盐(NO3-)转化为铵盐(NH4+)而去除掉,FeO(OH)不导电,加入Fe2+可能发生的反应是Fe2+能与FeO(OH)反应生成Fe3O4和氢离子,离子方程式为:Fe2++2FeO(OH)=Fe3O4+2H+,Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移,故C正确;
D.由图可知,PH=2.5时,NO3-的去除率达100%,PH=4.5NO3-的去除率约50%,所以溶液中H+浓度越大,对NO3-的去除率越高,故D正确;
故选B.
点评 本题考查水体中硝酸盐(NO3-)的处理,阅读摄取题干信息是解答关键,题目难度中等.

练习册系列答案
相关题目
5.在一定条件下,氯气与碘单质反应,可得到红棕色液体ICl.ICl可发生如下反应:
①2ICl+2Zn═ZnCl2+ZnI2;
②ICl+H2O═HCl+HIO
下列叙述不正确的是( )
①2ICl+2Zn═ZnCl2+ZnI2;
②ICl+H2O═HCl+HIO
下列叙述不正确的是( )
| A. | ICl中含有极性共价键 | |
| B. | 反应①中,当转移0.4mol电子时生成13.6g ZnCl2 | |
| C. | 反应②中,ICl既是氧化剂又是还原剂 | |
| D. | ICl与NaOH反应的化学方程式是:ICl+2NaOH═NaCl+NaIO+H2O |
17.常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A. | FeCl3溶液中:K+、Na+、SO42-、OH- | |
| B. | 使酚酞试液变红的溶液中:NH4+、Na+、HCO3-、NO3- | |
| C. | 漂白粉溶液中:H+、Na+、I-、Cl- | |
| D. | 与铝反应产生氢气的溶液中:Na+、K+、CO32-、OH- |
14.常温下,浓度均为0.1mol•L-1 的下列三种盐溶液,其pH 测定如表所示:
下列说法正确的是( )
| 序号 | ① | ② | ③ |
| 溶液 | CH3COONa | Na2CO3 | NaClO |
| pH | 8.8 | 11.6 | 10.3 |
| A. | 三种溶液中,水的电离程度①>③>② | |
| B. | Na2CO3 和NaHCO3 溶液中,粒子种类相同 | |
| C. | Na2CO3 溶液中,c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| D. | 常温下,等浓度的CH3COOH 溶液和HClO 溶液的酸性:HClO>CH3COOH |
1.2016年12月,中共中央、国务院印发了《关于全面推行河长制的意见》,进一步加强水污染治理工作.下列做法不应该提倡的是( )
| A. | 用碱性废水中和处理酸性废水 | |
| B. | 将工业废液排入海洋以减少河道污染 | |
| C. | 生活污水无害化处理后用于绿化灌溉 | |
| D. | 推广使用高效、低毒农药,减轻水体污染 |
19.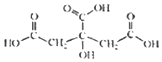 柠檬中含有的柠檬酸(其结构简式如下)对鲜切苹果具有较好的保鲜效果,可以在一段时间内防止鲜切苹果表面变色.下列说法不正确的是( )
柠檬中含有的柠檬酸(其结构简式如下)对鲜切苹果具有较好的保鲜效果,可以在一段时间内防止鲜切苹果表面变色.下列说法不正确的是( )
 柠檬中含有的柠檬酸(其结构简式如下)对鲜切苹果具有较好的保鲜效果,可以在一段时间内防止鲜切苹果表面变色.下列说法不正确的是( )
柠檬中含有的柠檬酸(其结构简式如下)对鲜切苹果具有较好的保鲜效果,可以在一段时间内防止鲜切苹果表面变色.下列说法不正确的是( )| A. | 柠檬酸的分子式是C6H8O7 | |
| B. | 柠檬酸是易溶于水的有机物 | |
| C. | 1mol柠檬酸足量的钠反应生成2.0mol的氢气 | |
| D. | 柠檬酸只能发生取代反应 |
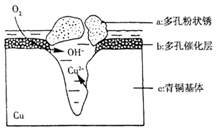 如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图.
如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图.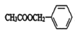 )存在于可可、咖啡、草莓等食品中,常用作食品香精.请回答下列问题:
)存在于可可、咖啡、草莓等食品中,常用作食品香精.请回答下列问题: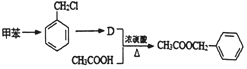
 的反应条件为光照
的反应条件为光照 生成D的反应化学方程式为
生成D的反应化学方程式为