题目内容
某温度下,在45.7g水中溶解14.3g Na2CO3.10H2O恰好达到饱和,该溶液密度为1.50g/cm3,求:
(1)该温度下Na2CO3溶解度;
(2)该溶液中Na2CO3的物质的量浓度;
(3)取出20.0ml该溶液,稀释成浓度为0.500mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
14.3g Na2CO3.10H2O中碳酸钠的质量为14.3g×
 =5.3g,故含有水的质量为14.3g-5.3g=9g,
=5.3g,故含有水的质量为14.3g-5.3g=9g,故100g:S=(45.7g+9g):5.3g,解得S=9.69g,
答:该温度下碳酸钠的溶解度为9.69g;
(2)碳酸钠的物质的量为
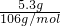 =0.05mol,
=0.05mol,溶液的体积为:
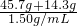 =40mL=0.04L,
=40mL=0.04L,故该饱和碳酸钠溶液的物质的量浓度为
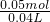 =1.25mol/L,
=1.25mol/L,答:该饱和碳酸钠溶液的物质的量浓度为1.25mol/L;
(3)根据稀释定律,稀释前后溶质的物质的量不变,令稀释后溶液的体积为V,则:
20mL×1.25mol/L=0.500mol/L×V,
解得V=50mL,
答:稀释后碳酸钠溶液的体积为50mL.
分析:(1)计算14.3g Na2CO3.10H2O中碳酸钠、水的质量,再根据溶解度定义计算100g水中溶解溶质的最大质量,即为该温度下的溶解度;
(2)根据n=
 计算碳酸钠的物质的量,根据V=
计算碳酸钠的物质的量,根据V=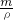 计算溶液的体积,再根据c=
计算溶液的体积,再根据c= 计算碳酸钠的物质的量浓度;
计算碳酸钠的物质的量浓度;(3)根据稀释定律,稀释前后溶质的物质的量不变,据此计算稀释后溶液的体积.
点评:本题考查溶解度计算、物质的量浓度的有关计算,难度不大,注意对溶解度的理解.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(12分)某温度时,在2L密闭容器中气态物质CO和H2反应生成气态物质Z,它们的物质的量随时间的变化如下表所示。
| t/min | CO/mol | H2/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.10 |
| 3 | 0.75 | 0.50 | 0.25 |
| 5 | 0.65 | 0.30 | 0.35 |
| 7 | 0.55 | 0.10 | 0.45 |
| 9 | 0.55 | 0.10 | 0.45 |
| 10 | 0.55 | 0.10 | 0.45 |
(1)(根据上表中数据,在下图中画出CO、z的物质的量的浓度(c)随时间(t)变化的曲线:
(2)体系中发生反应的化学方程式是 。
(3)在3—5 min时间内产物Z的平均反应速率: 。
(4)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。该反应是 (填“吸热”或“放热”)反应,反应的热化学方程式是 。
(5)恒容条件下,下列措施中能使n(CH3OH)/n(CO)增大的有 (选填序号)。
a.升高温度 b.使用催化剂 C.再充人2 mol H2 d.再充人2 mol He
(12分)某温度时,在2L密闭容器中气态物质CO和H2反应生成气态物质Z,它们的物质的量随时间的变化如下表所示。
|
t/min |
CO/mol |
H2/mol |
Z/mol |
|
0 |
1.00 |
1.00 |
0.00 |
|
1 |
0.90 |
0.80 |
0.10 |
|
3 |
0.75 |
0.50 |
0.25 |
|
5 |
0.65 |
0.30 |
0.35 |
|
7 |
0.55 |
0.10 |
0.45 |
|
9 |
0.55 |
0.10 |
0.45 |
|
10 |
0.55 |
0.10 |
0.45 |
(1)(根据上表中数据,在下图中画出CO、z的物质的量的浓度(c)随时间(t)变化的曲线:

(2)体系中发生反应的化学方程式是 。
(3)在3—5 min时间内产物Z的平均反应速率: 。
(4)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。该反应是 (填“吸热”或“放热”)反应,反应的热化学方程式是 。
(5)恒容条件下,下列措施中能使n(CH3OH)/n(CO)增大的有 (选填序号)。
a.升高温度 b.使用催化剂 C.再充人2 mol H2 d.再充人2 mol He
某温度时,在2L密闭容器中气态物质CO和H2反应生成气态物质Z,它们的物质的量随时间的变化如下表所示。
| t/min | CO/mol | H2/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.10 |
| 3 | 0.75 | 0.50 | 0.25 |
| 5 | 0.65 | 0.30 | 0.35 |
| 7 | 0.55 | 0.10 | 0.45 |
| 9 | 0.55 | 0.10 | 0.45 |
| 10 | 0.55 | 0.10 | 0.45 |
(1)(根据上表中数据,在下图中画出CO、z的物质的量的浓度(c)随时间(t)变化的曲线:

(2)体系中发生反应的化学方程式是 。
(3)在3—5 min时间内产物Z的平均反应速率: 。
(4)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。该反应是 (填“吸热”或“放热”)反应,反应的热化学方程式是 。
(5)恒容条件下,下列措施中能使n(CH3OH)/n(CO)增大的有 (选填序号)。
a.升高温度 b.使用催化剂 C.再充人2 mol H2 d.再充人2 mol He
 (2012?河西区一模)碳和碳的化合物在生产、生活中的应用非常广泛,此方面的科学研究为当今提倡的“低碳生活方式”提供依据.请按要求回答下列问题:
(2012?河西区一模)碳和碳的化合物在生产、生活中的应用非常广泛,此方面的科学研究为当今提倡的“低碳生活方式”提供依据.请按要求回答下列问题:
 B.盐酸逐滴滴入碳酸钠溶液至恰好完全反应时溶液呈中性
B.盐酸逐滴滴入碳酸钠溶液至恰好完全反应时溶液呈中性