题目内容
11.下列条件中,两种气体所含原子数一定相等的是( )| A. | 同质量、不同密度的N2和CO | B. | 同温度、同体积的H2和N2 | ||
| C. | 同体积、同密度的C2H6和NO | D. | 同压强、同体积的N2O和CO2 |
分析 两瓶气体所含原子数一定相等,则含有原子物质的量相等.
A.N2和CO的摩尔质量相等,二者质量相同,则二者物质的量相等,且都是双原子分子,含有原子数目一定相等;
B.温度、体积相等,压强会影响气体的物质的量;
C.根据m=ρV判断C2H6和NO的质量关系,根据n=$\frac{m}{M}$计算各自物质的量,结合分子含有原子数目计算原子物质的量;
D.同压强、同体积,温度会影响气体的物质的量.
解答 解:两瓶气体所含原子数一定相等,则含有原子物质的量相等.
A.二者质量相等,摩尔质量相等为28g/mol,根据n=$\frac{m}{M}$可知,二者物质的量一定相等,二者都是双原子分子,含有原子数目一定相等,故A正确;
B.同温度、同体积的H2和N2,二者压强不一定相等,二者的物质的量不一定相等,含有原子数目不一定相等,故B错误;
C.同体积、同密度的C2H6和NO,二者质量相等,C2H6和NO含有原子数目之比=$\frac{1}{30}$×8:$\frac{1}{30}$×2=4:1,故C错误;
D.同压强、同体积的N2O和CO2,二者的温度不一定相等,二者的物质的量不一定相等,二者都是三原子分子,故含有原子数目不一定相等,故D错误,
故选A.
点评 本题考查物质的量有关计算、阿伏伽德罗定律及推论,难度不大,注意根据pV=nRT理解阿伏伽德罗定律及推论.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
2. 工业合成氨反应为:N2(g)+3H2(g)?2NH3(g),对其研究如下:
工业合成氨反应为:N2(g)+3H2(g)?2NH3(g),对其研究如下:
(1)已知H-H键能为436kJ•mol-1,N-H键能为391kJ•mol-1,N≡N键的键能是945.6kJ•mol-1,则上述反应的△H=-92.46kJ•mol-1.
(2)在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:
①该温度下,若向同容积的另一容器中投入的N2、H2、NH3浓度分别为3mol/L,3mol/L、3mol/L,此时v正大于v逆(填“大于”、“小于”或“等于”)
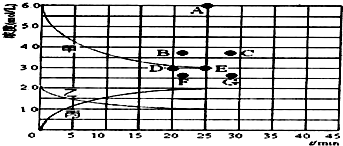
②由上述表中的实验数据计算得到“浓度~时间”的关系可用图中的曲线表示,表示c(N2)~t的曲线是乙.在此温度下,若起始充入4molN2和12molH2,反应刚达到平衡时,表示c(H2)的曲线上相应的点为B.
 工业合成氨反应为:N2(g)+3H2(g)?2NH3(g),对其研究如下:
工业合成氨反应为:N2(g)+3H2(g)?2NH3(g),对其研究如下:(1)已知H-H键能为436kJ•mol-1,N-H键能为391kJ•mol-1,N≡N键的键能是945.6kJ•mol-1,则上述反应的△H=-92.46kJ•mol-1.
(2)在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
②由上述表中的实验数据计算得到“浓度~时间”的关系可用图中的曲线表示,表示c(N2)~t的曲线是乙.在此温度下,若起始充入4molN2和12molH2,反应刚达到平衡时,表示c(H2)的曲线上相应的点为B.
19.下列有关物质浓度关系的描述中,正确的是( )
| A. | 25℃时,NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-7mol•L-1 | |
| B. | 25℃时,向0.1mol•L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) | |
| C. | 0.1mol•L-1的NaHCO3溶液中:c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) | |
| D. | 同温下,pH相同时,溶液物质的量浓度:c(CH3COONa)>c(NaHCO3)>c(Na2CO3)>c(C6H5ONa) |
3. 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法不正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法不正确的是( )
 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法不正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法不正确的是( )| A. | 1mol该有机物可与2mol钠反应 | |
| B. | 该有机物可以发生酯化、加成、醇催化氧化 | |
| C. | 1mol碳酸钠可与2mol该物质反应产生1mol二氧化碳 | |
| D. | 该有机物中含有碳碳双键、羟基、羧基等官能团 |
20.NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,28 g N2所含电子数为10NA | |
| B. | 46 g钠充分燃烧时转移电子数为2NA | |
| C. | 0.1 mol•L-1NH4Cl溶液中Cl-离子数为0.1NA | |
| D. | 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA |
1.用0.10mol/L H2SO4溶液滴定0.1mol/L的氨水,滴定的过程中不可能出现的结果是( )
| A. | c(NH4+)>c(SO42-),c(OH-)>c(H+) | B. | c(NH4+)=c(SO42-),c(OH-)=c(H+) | ||
| C. | c(NH4+)>c(SO42-),c(H+)>c(OH-) | D. | c(SO42-)>c(NH4+),c(H+)>c(OH-) |