题目内容
11.下列实验可达到实验目的是( )①将CH3-CH-CH3与NaOH醇溶液共热制备CH3─CH═CH2
②乙酰水杨酸
 与适量NaOH溶液反应制备
与适量NaOH溶液反应制备
③向CH3CH2Br中滴入AgNO3溶液以检验溴元素
④用溴的四氯化碳溶液吸收SO2气体.
| A. | ①④ | B. | ④③ | C. | 只有 ④ | D. | 全都不能 |
分析 ①NaOH的醇溶液共热是卤代烃消去反应的条件;
②酚羟基和羧基均具有酸性,可以和氢氧化钠发生中和反应;
③根据卤代烃中卤素原子的检验方法来回答;
④溴单质和二氧化硫的反应必须在水溶液中进行.
解答 解:①醇类物质在NaOH的醇溶液共热的条件不能发生反应,条件应为浓硫酸并加热,故①错误;
②乙酰水扬酸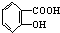 与适量NaOH溶液反应生成的是
与适量NaOH溶液反应生成的是 ,故②错误;
,故②错误;
③向CH3CH2Br中先加入氢氧化钠,再加入硝酸酸化的硝酸银以检验溴元素,故③错误;
④溴单质和二氧化硫的反应必须在水溶液中进行,在四氯化碳中不会发生反应,故④错误.
故选D.
点评 本题考查化学实验方案的评价,以实验形式考查物质的性质,注意在解此类题时,首先需要知道物质发生反应的条件,熟记各官能团的性质是解题的关键,难度不大.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
16.下列叙述不正确的是( )
| A. | 液态氯化氢不导电,说明它是共价化合物 | |
| B. | 若电解质溶液中分子和离子同时存在,电离方程中只能采用“?”表示 | |
| C. | 相同条件下,强电解质溶液的导电性一定比弱电解质溶液强 | |
| D. | 物质导电的本质是存在自由移动的离子 |
19.相同温度下等物质的量浓度的下列溶液中,pH值最大的是 ( )
| A. | NH4Cl | B. | NH3.H2O | C. | NH4HSO4 | D. | (NH4)2SO4 |
6.下列有关平衡常数的说法中不正确的是( )
| A. | 温度一定时,一个给定的化学反应的平衡常数是一个常数 | |
| B. | 改变反应物浓度或生成物浓度会改变平衡常数 | |
| C. | 温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数 | |
| D. | 浓度Qc<K时,反应向正反应方向进行 |
3.下列关于环境问题的说法不正确的是( )
| A. | pH小于5.6的降雨称为酸雨 | |
| B. | 充分利用太阳能有助于“节能减排” | |
| C. | 在燃煤中加入适量石灰石,有助于环境保护 | |
| D. | 含磷洗涤剂易被细菌分解,不会导致水体污染 |
1.下列有关概念间关系的说法正确的是( )
| A. | 失电子越多,还原性就一定越强 | |
| B. | 某元素由单质变为化合物,该元素有可能被氧化也有可能被还原 | |
| C. | 某物质焰色反应呈黄色,该物质一定含钠单质,可能含钾单质 | |
| D. | 金属氧化物一定是碱性氧化物 |
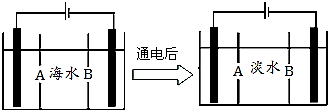 南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水.
南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水.