题目内容
7.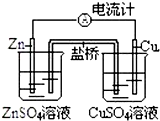 在如图装置中,Zn为负极,电极反应式为Zn-2e-═Zn2+,Cu电极的电极反应式为Cu2++2e-═Cu;盐桥(含KCl饱和溶液)中移向左边烧杯的离子为氯离子,电流从Zn极(填“Cu”或者“Zn”)流出.
在如图装置中,Zn为负极,电极反应式为Zn-2e-═Zn2+,Cu电极的电极反应式为Cu2++2e-═Cu;盐桥(含KCl饱和溶液)中移向左边烧杯的离子为氯离子,电流从Zn极(填“Cu”或者“Zn”)流出.
分析 锌比铜活泼,形成原电池反应时锌为负极,被氧化,铜为正极,正极发生还原反应,原电池工作时阳离子向正极移动,以此解答该题.
解答 解:锌比铜活泼,形成原电池反应时锌为负极,被氧化,铜为正极,正极发生还原反应,原电池工作时阳离子向正极移动,所以锌为负极,电极反应式为:Zn-2e-═Zn2+,铜为正极,Cu电极发生为Cu2++2e-═Cu,盐桥(含KCl饱和溶液)中移向负极左边烧杯的离子为:氯离子;电流从负极Zn 极流出,故答案为:负;Zn-2e-═Zn2+;Cu2++2e-═Cu;氯离子;Zn.
点评 本题考查原电池和电解池的工作原理,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握基础知识的积累,掌握电极反应式的书写.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
17.甲苯的一氯代物有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
18.乙酸分子结构中,含有的σ键和π键的个数分别是( )
| A. | 7、1 | B. | 6、2 | C. | 3、5 | D. | 4、4 |
2.下列叙述正确的是( )
| A. | 单质分子中不一定存在化学键 | |
| B. | 离子化合物中只含离子键,不含共价键 | |
| C. | 共价化合物一定含共价键,可能含离子键 | |
| D. | 非金属元素组成的化合物不存在离子键 |
12.下列说法中不正确的是( )
| A. | 相对分子质量相同的不同物质一定是同分异构体 | |
| B. | 分子式相同而分子结构不相同的有机化合物是同分异构体 | |
| C. | 每个碳原子的化合价都已“饱和”,碳原子之间只以单键相结合的链烃,一定是烷烃 | |
| D. | 分子式相同,结构又相同的有机化合物,一定是同一物质 |
19.1mol某饱和烷烃在氧气中充分燃烧,需要消耗氧气246.4L(标准状况下).它在光照的条件下与氯气反应能生成3种不同的一氯取代物.该烃的结构简式是( )
| A. | 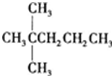 | B. | CH3CH2CH2CH2CH3 | C. | 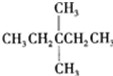 | D. | 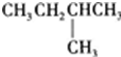 |
16.下列各组离子在给定条件下能大量共存的是( )
| A. | 在pH=1的溶液中:NH4+、K+、ClO-、SO32- | |
| B. | 有CO32-存在的溶液中:Na+、Mg2+、Ca2+、NO3- | |
| C. | 有MnO4-存在的酸性溶液中:Na+、Ba2+、Cl-、I- | |
| D. | 在c(H+):c(OH-)=1:10的水溶液中:Na+、SO42-、K+、S2- |
19.关于下列各组物质的叙述,正确的是( )
①H2N-CH2-COOH和H3C-CH2-NO2
②CH3COOH和HCOOCH3
③CH3CH2CHO 和 CH3COCH3
④CH3CH2CH2OH和CH3CH2OCH3
⑤2-甲基丙烷和丁烷
⑥CH3CH=CHCH2CH3和CH3CH2CH2CH=CH2
⑦CH3(CH2)4CH3 和 CH3CH(CH3)CH2CH3.
①H2N-CH2-COOH和H3C-CH2-NO2
②CH3COOH和HCOOCH3
③CH3CH2CHO 和 CH3COCH3
④CH3CH2CH2OH和CH3CH2OCH3
⑤2-甲基丙烷和丁烷
⑥CH3CH=CHCH2CH3和CH3CH2CH2CH=CH2
⑦CH3(CH2)4CH3 和 CH3CH(CH3)CH2CH3.
| A. | ①②③④⑤⑥⑦都是同分异构体 | B. | ⑥是官能团异构类型 | ||
| C. | ⑦是碳链异构类型 | D. | ①②③④是官能团异构类型 |