题目内容
4.下列关于2SO2(g)+O2(g)?2SO3(g)△H<0反应的图象中,不正确的是( )| A. |  | B. |  | C. | 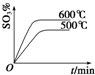 | D. | 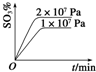 |
分析 A.反应是放热反应,随温度升高正逆反应速率增大,平衡逆向进行;
B.图中分析可知三氧化硫含量开始增大反应正向进行,达到平衡状态,随温度升高平衡逆向进行,三氧化硫含量减小;
C.先拐先平温度高,温度越高平衡逆向进行三氧化硫含量减小;
D.先拐先平压强大,压强越大平衡向气体体积减小的方向进行,平衡正向进行,三氧化硫含量增大.
解答 解:A.2SO2(g)+O2(g)?2SO3(g)△H<0,反应是放热反应,随温度升高正逆反应速率增大,平衡逆向进行,逆反应速率大于正反应速率,图象符合,故A正确;
B.图中分析可知三氧化硫含量开始增大反应正向进行,达到平衡状态,随温度升高向吸热反应方向进行,平衡逆向进行,三氧化硫含量减小,图象变化曲线符合,故B正确;
C.先拐先平温度高,温度越高平衡越向吸热反应方向进行,平衡逆向进行三氧化硫含量减小,图象中曲线变化不符合,故C错误;
D.先拐先平压强大,压强越大平衡向气体体积减小的方向进行,平衡正向进行,三氧化硫含量增大,图象变化符合要求,故D正确;
故选C.
点评 本题考查了化学平衡、反应速率图象分析判断,主要是反应特征和化学平衡移动原理的理解应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
3.下列说法正确的是( )
| A. | 配制Na2S溶液时,为了抑制S2-的水解,常加入少量氢氧化钠 | |
| B. | 明矾用于净水过程只发生物理变化 | |
| C. | 把纯水加热水的电离程度增大,但水仍然是中性的,pH=7 | |
| D. | 加热蒸发AlCl3饱和溶液得纯净的AlCl3晶体 |
15.在常温下,下列溶液中有关微粒浓度的关系正确的是( )
| A. | 0.1mol•L-1(NH4)2Fe(SO4)2溶液:c (SO42-)>c(NH4+)>c(Fe2+)>c(H+) | |
| B. | 0.1mol•L-1pH为4的NaHSO3溶液中:c(HSO3-)>c(H2SO3)>c(SO32-) | |
| C. | 0.1 mol•L-1 Na2S溶液中:2c(Na+)═c(S2-)+c(HS-)+c(H2S) | |
| D. | 某二元弱酸的酸式盐NaHA溶液:c(Na+)+c(H+)═c(OH-)+c(HA-)+c(A2-) |
12.在通常条件下,NO2和SO2可以很容易发生反应生成NO和SO3.现将碳跟浓硫酸共热产生的气体X和碳跟浓硝酸共热产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )

| A. | 洗气瓶中产生的沉淀是碳酸钡 | |
| B. | 洗气瓶中产生的沉淀是硫酸钡 | |
| C. | 在Z导管出来的气体中无二氧化碳 | |
| D. | 反应一段时间后洗气瓶中溶液的酸性减弱 |
19.如图所示的实验操作错误的是( )
| A. |  | B. | 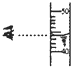 | C. |  | D. | 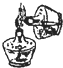 |
9. 已知:①CO(g)+H2O(g)?H2(g)+CO2(g);△H=-41.2kJ/mol
已知:①CO(g)+H2O(g)?H2(g)+CO2(g);△H=-41.2kJ/mol
②CH4(g)+CO2(g)?2CO(g)+2H2(g);△H=+247.3kJ/mol
③CH4(g)+H2O(g)?3H2(g)+CO(g);△H3
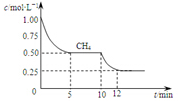
若反应③在1升容器中进行,测得CH4的物质的量浓度随反应时间的变化如图所示.下列有关叙述错误的是( )
 已知:①CO(g)+H2O(g)?H2(g)+CO2(g);△H=-41.2kJ/mol
已知:①CO(g)+H2O(g)?H2(g)+CO2(g);△H=-41.2kJ/mol②CH4(g)+CO2(g)?2CO(g)+2H2(g);△H=+247.3kJ/mol
③CH4(g)+H2O(g)?3H2(g)+CO(g);△H3
若反应③在1升容器中进行,测得CH4的物质的量浓度随反应时间的变化如图所示.下列有关叙述错误的是( )
| A. | △H3=+206kJ/mol | |
| B. | 反应③进行到10min时,改变的外界条件可能是升高温度 | |
| C. | 反应③进行过程中,0~5min这段时间共吸收的热量为103.05kJ | |
| D. | 当反应③平衡后,向容器中通入CH4,平衡向正反应方向移动,CH4的转化率将增大 |
13.下列各组中均为两瓶无标签的无色溶液,不许使用其它任何试剂(包括水),也能鉴别出来的是( )
①NaOH和Al2(SO4)3②Na2CO3和盐酸③NaHCO3和盐酸④盐酸和NaAlO2.
①NaOH和Al2(SO4)3②Na2CO3和盐酸③NaHCO3和盐酸④盐酸和NaAlO2.
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②④ |
14.在相同条件下能进行如下三个反应:
2A-+B2═2B-+A2
2C-+A2═2A-+C2
2B-+D2═2D-+B2
由此可判断以下分析正确的是( )
2A-+B2═2B-+A2
2C-+A2═2A-+C2
2B-+D2═2D-+B2
由此可判断以下分析正确的是( )
| A. | 氧化性:A2>B2>C2>D2 | B. | 还原性:C->A->B->D- | ||
| C. | 2A-+D2═2D-+A2的反应能进行 | D. | 2C-+B2═2B-+C2的反应不能进行 |