题目内容
4.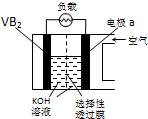 硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时反应为:4VB2+11O2═4B2O3+2V2O5.下列说法正确的是( )
硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时反应为:4VB2+11O2═4B2O3+2V2O5.下列说法正确的是( )| A. | 电极a为电池正极 | |
| B. | 图中选择性透过膜只能让阳离子选择性透过 | |
| C. | 电子由VB2极经KOH溶液流向a电极 | |
| D. | VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O |
分析 硼化钒-空气燃料电池中,VB2在负极失电子,氧气在正极上得电子,电池总反应为:4VB2+11O2→4B2O3+2V2O5;氧气在正极得电子生成氢氧根离子,溶液中阴离子向负极移动.
解答 解:A、硼化钒-空气燃料电池中,VB2在负极失电子,氧气在正极上得电子,所以a为正极,故A正确;
B、氧气在正极上得电子生成OH-,OH-通过选择性透过膜向负极移动,故B错误;
C、“电子不下水”,电子只在导线中移动,不能在溶液中移动,故C错误;
D、负极上是VB2失电子发生氧化反应,则VB2极发生的电极反应为:2VB2+22OH--22e-→V2O5+2B2O3+11H2O,故D正确;
故选AD.
点评 本题考查原电池的工作原理,题目难度不大,本题注意把握电极反应式的书写,正确判断离子的定向移动.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列各组内的物质中互为同系物的是( )
| A. | CH3CH=CH2和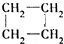 | B. | CH3CH2CH2CH3和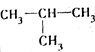 | C. | CH3Cl和CH3CH2Br | D. | CH3OH和CH3CH2OH |
19.下列有关物质用途的叙述中,错误的是( )
| A. | 液氨常被用作制冷剂 | |
| B. | 可利用2Fe3++Cu═Cu2++2Fe2+腐蚀印刷电路板 | |
| C. | 为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质 | |
| D. | 已知3Cl2+2NH3═N2+6HCl,工业上可用浓氨水检查氯气管道是否漏气 |
9.下列各组离子中,能在水溶液中大量共存的是( )
| A. | Na+、H+、Cl-、HCO3- | B. | Na+、Fe2+、Cl-、OH- | ||
| C. | NH4+、CO32-、NO3-、Ba2+ | D. | Cu2+、Fe3+、Mg2+、SO42- |
16.将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).判断该分解反应已经达到化学平衡的是( )
| A. | 2v(NH3)=v(CO2) | B. | 密闭容器中c(NH3):c(CO2)=2:1 | ||
| C. | 密闭容器中体积不变 | D. | 密闭容器中混合气体的密度不变 |
13.下列颜色变化与氧化还原反应无关的是( )
| A. | 乙醇使酸性K2Cr2O7溶液由橙色变为绿色 | |
| B. | 向品红溶液中通入SO2气体,品红褪色,加热后又恢复红色 | |
| C. | 将铜丝在空气中烧黑后.趁热插入乙醇中又变红 | |
| D. | 将乙醛加人到新制Cu(OH)2悬浊液中并加热至沸腾,出现红色沉淀 |
14.将X气体通人BaCl2溶液中,未见沉淀生成.但若将X和SO2,同时通人BaCl2溶液中.就有沉淀生成.则X气体不可能是( )
| A. | CO2 | B. | NH3 | C. | Cl2 | D. | NO2 |