题目内容
下列表示对应化学反应的离子方程式正确的是( )
| A、用过量NaOH溶液吸收SO2:OH-+SO2=HSO3- |
| B、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| C、Fe3O4溶于稀盐酸:Fe3O4+8H+=3Fe2++4H2O |
| D、NaHSO4溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、用过量NaOH生成亚硫酸盐;
B、少量要符合组成之比;
C、不符合客观事实,生成物质中还有铁离子;
D、假设NaHSO4为1mol,使原溶液中的SO42-恰好完全沉淀,需要Ba(OH)21mol,根据各离子的物质的量判断反应的程度,以此书写离子方程式.
B、少量要符合组成之比;
C、不符合客观事实,生成物质中还有铁离子;
D、假设NaHSO4为1mol,使原溶液中的SO42-恰好完全沉淀,需要Ba(OH)21mol,根据各离子的物质的量判断反应的程度,以此书写离子方程式.
解答:
解:A、用过量NaOH生成亚硫酸盐,正确的离子方程式为2OH-+SO2=H2O+SO32-,故A错误;
B、少量要符合组成之比,把少的当作1mol,正确的离子方程式为HCO3-+Ca2++OH-=CaCO3↓+H2O,故B正确;
C、不符合客观事实,生成物质中还有铁离子,离子方程式中应写成化学式,离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O,故C错误;
D、设NaHSO4为1mol,使原溶液中的SO42-恰好完全沉淀,需要Ba(OH)21mol,则发生反应的离子的物质的量分别为1mol,离子方程式为H++SO42-+Ba2++OH-=BaSO4↓+H2O,故D错误;
故选B.
B、少量要符合组成之比,把少的当作1mol,正确的离子方程式为HCO3-+Ca2++OH-=CaCO3↓+H2O,故B正确;
C、不符合客观事实,生成物质中还有铁离子,离子方程式中应写成化学式,离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O,故C错误;
D、设NaHSO4为1mol,使原溶液中的SO42-恰好完全沉淀,需要Ba(OH)21mol,则发生反应的离子的物质的量分别为1mol,离子方程式为H++SO42-+Ba2++OH-=BaSO4↓+H2O,故D错误;
故选B.
点评:本题考查离子方程式的书写,题目难度不大,注意从化学式、离子符号、电荷守恒以及是否符合反应实际的角度分析.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
下列分子中属于含极性键的非极性分子的是( )
| A、H2S |
| B、CH4 |
| C、Cl2 |
| D、NH3 |
下列物质转化需要加入还原剂才能实现的是( )
| A、CuO→Cu |
| B、Fe2+→Fe3+ |
| C、NaOH→NaCl |
| D、KClO3→KCl |
A、B、C、D、E是元素周期表中的短周期主族元素,且原子序数依次增大.已知A与B不在同周期,A与C同主族,B原子最外层电子数是其电子层数的2倍,A、C、E原子最外层电子数之和为6,D的氧化物具有两性.下列说法正确的是( )
| A、A、B只能形成一种化合物 |
| B、离子半径:C<D |
| C、气态氢化物的稳定性:B>E |
| D、元素C、D的最高价氧化物对应水化物之间不能发生反应 |
下列有关物质分类的说法,不正确的是( )
| A、CO2是酸性氧化物,也是非金属氧化物 |
| B、KNO3是钾盐、硝酸盐,也是正盐 |
| C、H2SO4是含氧酸、二元酸,也是强酸 |
| D、NH3?H2O是一元强碱,也是可溶性碱 |
在无色透明的溶液中可以大量共存的离子组是( )
| A、OH-、K+、Al3+ |
| B、OH-、Cl-、NH4+ |
| C、Cu2+、NO3-、Cl- |
| D、Mg2+、K+、Cl- |
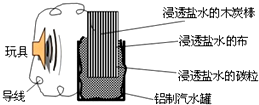 利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置,如图就是用一个废旧材料制作的可用于驱动玩具电池的示意图.该电池工作时有关说法正确的是( )
利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置,如图就是用一个废旧材料制作的可用于驱动玩具电池的示意图.该电池工作时有关说法正确的是( )| A、铝罐将逐渐被腐蚀 |
| B、该装置实现了化学能向电能的转化 |
| C、炭棒应与玩具电机的负极相连 |
| D、该电池工作一段时间后炭棒和炭粒的质量会减轻 |
下列基态原子的电子构型中,正确的是( )
| A、3d94s2 |
| B、3d44s2 |
| C、3d104s0 |
| D、3d83s2 |
NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、0.1molFe和足量浓硝酸反应后,转移电子数目为0.3NA |
| B、标准状况下,1 molHF分子体积约为22.4 L |
| C、1molCl2参加化学反应,一定转移2mol电子 |
| D、11g 2D218O中含有的氢氧键数目为NA |