题目内容
(8分)常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L HCl溶液和
20.00 mL 0.1000 mol/L CH3COOH溶液,得到2条滴定曲线,如下图所示:
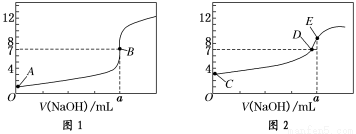
(1)由A、C点判断,滴定HCl溶液的曲线是______(填“图1”或“图2”);
(2)a=________ mL;
(3)c(Na+)=c(CH3COO-)的点是________;
(4)E点对应离子浓度由大到小的顺序为________________。
(1)图1 (2)20.00 (3)D (4)c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
【解析】
试题分析:(1)如果酸为强酸,则0.1000mol/L酸的pH为1,根据酸的初始pH知,图1为盐酸滴定曲线;
(2)滴定20.00mL 0.1000mol/L HCl溶液,NaOH和HCl恰好反应时,消耗20mlNaOH溶液,生成强酸强碱盐,溶液呈中性,滴定终点时n(HCl)=n(NaOH),则a=20.00mL;
(3)c(Na+)=c(CH3COO-),溶液中存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以c(OH-)=c(H+),则溶液呈中性,pH=7,故点D符合题意;
(4)根据图1知,a点氢氧化钠溶液的体积是20mL,酸和碱的物质的量相等,二者恰好反应生成盐,醋酸钠为强碱弱酸盐,其溶液呈碱性,所以c(OH-)>c(H+),溶液中存在电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以c(Na+)>c(CH3COO-),盐类水解程度较小,所以c(CH3COO-)>c(OH-),则溶液中离子浓度大小顺序是c(Na+)>c(CH3COO-)>c(OH-)>c(H+)。

在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/(mol·L-1) | 0.1 | 0.2 | 0 |
平衡浓度/(mol·L-1) | 0.05 | 0.05 | 0.1 |
下列说法错误的
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z,其平衡常数为1 600
2Z,其平衡常数为1 600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数

 ,有关说法正确的是
,有关说法正确的是
 (Ⅱ)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
(Ⅱ)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系: CO2(g)+3H2(g) ΔH>0。
CO2(g)+3H2(g) ΔH>0。

 M2+(aq) +2OH— (aq),溶液的pH=a,则其Ksp= 。
M2+(aq) +2OH— (aq),溶液的pH=a,则其Ksp= 。 ],又知100℃时,水的离子积常数为1×10—12,25℃时纯水的AG1和100℃时食盐水的AG2的关系为:AG1 AG2(=、<、>);在100℃时将V1ml AG=8的硫酸与V2ml AG=—6的烧碱溶液混合后AG=0,则V1:V2= 。
],又知100℃时,水的离子积常数为1×10—12,25℃时纯水的AG1和100℃时食盐水的AG2的关系为:AG1 AG2(=、<、>);在100℃时将V1ml AG=8的硫酸与V2ml AG=—6的烧碱溶液混合后AG=0,则V1:V2= 。