题目内容
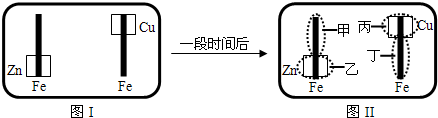
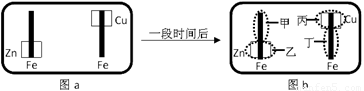
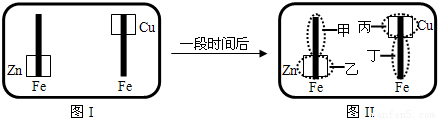
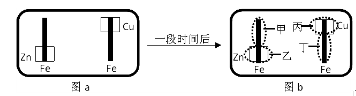
已知Fe2+可用K3Fe(CN)6来检验(呈蓝色).将图I装置中的铁棒末段分别联上一块锌片和铜片,并静置于含有K3Fe(CN)6及酚酞的混合凝胶上.一段时间后发现凝胶的某些区域(如图II示)发生了变化.则下列说法正确的是( )
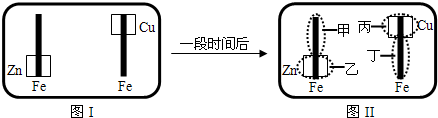

| A.甲区不变色 | B.乙区呈现蓝色 |
| C.丙区产生Cu2+离子 | D.丁区产生Fe2+离子 |
A、甲区发生电极反应:O2+2H2O+4e-=4OH-,生成的氢氧根离子能使酚酞变红色,所以甲极区变红色,故A错误;
B、乙区发生电极反应:2Zn-4e-=2Zn2+,所以乙极区不变色,故B错误;
C、丙区发生电极反应:O2+2H2O+4e-=4OH-,不会产生铜离子,故C错误;
D、丁区发生电极反应:2Fe-4e-=2Fe2+,故D正确.
故选D.
B、乙区发生电极反应:2Zn-4e-=2Zn2+,所以乙极区不变色,故B错误;
C、丙区发生电极反应:O2+2H2O+4e-=4OH-,不会产生铜离子,故C错误;
D、丁区发生电极反应:2Fe-4e-=2Fe2+,故D正确.
故选D.

练习册系列答案
相关题目