题目内容
6.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 1molNa与乙醇完全反应,失去2NA电子 | |
| B. | 常温常压下,8gCH4含有5NA个电子 | |
| C. | 6.0g冰醋酸与4.6g乙醇反应生成乙酸乙酯的分子数为0.1 NA | |
| D. | 标准状况下,22.4L苯含有NA个C6H6分子 |
分析 A、钠和乙醇反应后变为+1价;
B、求出甲烷的物质的量,然后根据甲烷为10电子分子来分析;
C、酯化反应为可逆反应;
D、标况下苯为液态.
解答 解:A、钠和乙醇反应后变为+1价,故1mol钠和乙醇反应失去NA个电子,故A错误;
B、8g甲烷的物质的量为0.5mol,而甲烷为10电子分子,故0.5mol甲烷中含5NA个电子,故B正确;
C、酯化反应为可逆反应,不能进行彻底,故生成的乙酸乙酯分子个数小于0.1NA个,故C错误;
D、标况下苯为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.LED灯既能节能、亮度又好.图是某课外活动小组设计的用化学电源使LED灯发光的装置.下列说法正确的是( )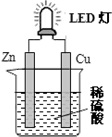

| A. | 锌片表面有气泡生成 | |
| B. | 装置中存在“化学能→电能→光能”的转换 | |
| C. | 如果将硫酸换成柠檬汁,导线中就不会有电子流动 | |
| D. | 如果将铜片换成锌片,LED灯仍然会发光 |
14.苯与乙烯相比较,下列叙述不正确的是( )
| A. | 都能在空气中燃烧 | |
| B. | 都容易发生取代反应 | |
| C. | 苯和乙烯都能在一定条件下发生加成反应 | |
| D. | 苯不能使酸性KMnO4溶液褪色而乙烯能 |
1. 用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法错误的是( )
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法错误的是( )
 用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法错误的是( )
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法错误的是( )| A. | 构成原电池时b极反应为Cu2++2e-═Cu | |
| B. | 构成电解池时a极质量一定减少 | |
| C. | 构成电解池时b极质量可能减少也可能增加 | |
| D. | 构成的原电池或电解池工作后可能产生大量气体 |
11.关于下列一组图示的说法中正确的是( )
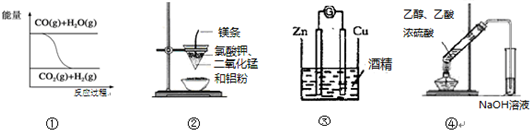

| A. | 图①表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”为吸热反应 | |
| B. | 图②可以制取金属锰 | |
| C. | 图③形成原电池 | |
| D. | 图④制取乙酸乙酯 |
15.如表为元素周期表的一部分,X、Y、Z、W为短周期元素,其中X元素的原子最外层电子数是其内层电子数的2倍.下列说法正确的是( )
| X | Y | ||
| Z | W | ||
| T |
| A. | Y氢化物的沸点一定比X氢化物的沸点高 | |
| B. | Z的最高价氧化物的水化物酸性比W的强 | |
| C. | XZ2、XW4 与Na2O的化学键类型相同 | |
| D. | 根据元素周期律,可以推测存在TZ2和TW4 |
16.已知:①C(s)+$\frac{1}{2}$O2(g)═CO(g);△H=-110.5kJ•mol-1
②C(s)+O2(g)═CO2(g);△H=-393.51kJ•mol-1
则反应C(s)+CO2(g)═2CO(g)的△H为( )
②C(s)+O2(g)═CO2(g);△H=-393.51kJ•mol-1
则反应C(s)+CO2(g)═2CO(g)的△H为( )
| A. | -283.01 kJ•mol-1 | B. | +172.51 kJ•mol-1 | ||
| C. | +283.01 kJ•mol-1 | D. | -172.51 kJ•mol-1 |

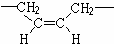 ,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为10002.
,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为10002.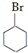 +NaOH$\stackrel{△}{→}$
+NaOH$\stackrel{△}{→}$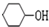 +NaBr.
+NaBr.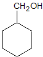 的合成路线.
的合成路线.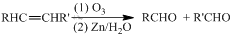 (R,R’代表烃基或氢)CH2=CHCH=CH2$\stackrel{催化剂}{→}$
(R,R’代表烃基或氢)CH2=CHCH=CH2$\stackrel{催化剂}{→}$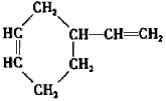

 $→_{催化剂}^{氢气}$
$→_{催化剂}^{氢气}$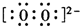 .
.