题目内容
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似,又已知AlCl3熔沸点较低,易升华.试回答下列问题:
(1)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式 .
(2)Be(OH)2与Mg(OH)2可用试剂 鉴别,其离子方程式为 .
(3)BeCl2是 化合物(填写“离子”或“共价”).
(4)Li与Mg根据对角线规则,性质也相似,则Li在空气中燃烧,主要产物的化学式是 .
(1)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式
(2)Be(OH)2与Mg(OH)2可用试剂
(3)BeCl2是
(4)Li与Mg根据对角线规则,性质也相似,则Li在空气中燃烧,主要产物的化学式是
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:(1)元素周期表中,处于对角线位置的元素具有相似的性质,则根据铝的单质的性质可推断铍与氢氧化钠的反应,据此解答;
(2)氢氧化铍与氢氧化铝性质相似,能和氢氧化钠反应,而Mg(OH)2和氢氧化钠不反应;
(3)氯化铍与氯化铝相似,均为共价化合物;
(4)Li与Mg根据对角线规则,性质也相似,而Mg与空气中的氧气、氮气反应,主要生成MgO,还有少量Mg3N2生成,则Li在空气中燃烧,主要生成氧化锂.
(2)氢氧化铍与氢氧化铝性质相似,能和氢氧化钠反应,而Mg(OH)2和氢氧化钠不反应;
(3)氯化铍与氯化铝相似,均为共价化合物;
(4)Li与Mg根据对角线规则,性质也相似,而Mg与空气中的氧气、氮气反应,主要生成MgO,还有少量Mg3N2生成,则Li在空气中燃烧,主要生成氧化锂.
解答:
解:(1)金属铍与铝的单质及其化合物性质相似,则Be与NaOH溶液反应生成Na2BeO2和氢气,离子反应为Be+2OH-=BeO22-+H2↑,故答案为:Be+2OH-=BeO22-+H2↑;
(2)氢氧化铍与氢氧化铝性质相似,能和氢氧化钠反应,而Mg(OH)2和氢氧化钠不反应,则选NaOH溶液鉴别,离子反应为Be(OH)2+2OH-=BeO22-+2H2O,故答案为:NaOH溶液;Be(OH)2+2OH-=BeO22-+2H2O;
(3)氯化铍与氯化铝相似,均为共价化合物,故答案为:共价;
(4)Li与Mg根据对角线规则,性质也相似,而Mg与空气中的氧气、氮气反应,主要生成MgO,还有少量Mg3N2生成,则Li在空气中燃烧,主要生成Li2O,还生成少量的Li3N,故答案为:Li2O.
(2)氢氧化铍与氢氧化铝性质相似,能和氢氧化钠反应,而Mg(OH)2和氢氧化钠不反应,则选NaOH溶液鉴别,离子反应为Be(OH)2+2OH-=BeO22-+2H2O,故答案为:NaOH溶液;Be(OH)2+2OH-=BeO22-+2H2O;
(3)氯化铍与氯化铝相似,均为共价化合物,故答案为:共价;
(4)Li与Mg根据对角线规则,性质也相似,而Mg与空气中的氧气、氮气反应,主要生成MgO,还有少量Mg3N2生成,则Li在空气中燃烧,主要生成Li2O,还生成少量的Li3N,故答案为:Li2O.
点评:本题考查元素周期表及应用,侧重学生分析能力及知识迁移应用能力的考查,注意利用已知物质的性质进行类别解答,注意物质的相似之处和不同之处,难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
口香糖中常用木糖醇做甜味剂,木糖醇可以防止龋齿,木糖醇的结构简式为: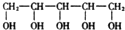 ,下列有关木糖醇的说法正确的是( )
,下列有关木糖醇的说法正确的是( )
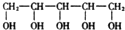 ,下列有关木糖醇的说法正确的是( )
,下列有关木糖醇的说法正确的是( )| A、木糖醇是-种单糖,不能发生水解反应 |
| B、木糖醇易溶解于水,不能发生酯化反应 |
| C、木糖醇在口腔中不易被氧化为酸 |
D、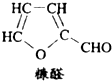 木糖醇脱去三分子水可得糠醛(结构如图) |
禁止使用含磷洗衣粉(三聚磷酸钠Na5P3O10)原因是( )
| A、会刺激皮肤 |
| B、会腐蚀下水道 |
| C、会引起白色污染 |
| D、会造成水质富营养化,使水质变坏 |
SO2 通入滴有酚酞的NaOH溶液中,发现红色消失.主要原因是( )
| A、SO2有漂白性 |
| B、SO2溶于水后,溶液呈酸性 |
| C、SO2有还原性 |
| D、SO2有氧化性 |
若溶液中由水电离产生的c(OH-)=1×10-14mol?L-1,满足条件的溶液中一定可以大量共存的离子组是( )
| A、Al3+,Na+,NO3-,Cl- |
| B、K+,Na+,Cl-,NO3- |
| C、K+,Na+,Cl-,CH3COO- |
| D、K+,NH4+,SO42-,NO3- |
下列离子方程式正确的是( )
| A、三氯化铝溶液中加入过量NaOH溶液:Al3++3OH-═Al(OH)3↓ |
| B、4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合:4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ |
| C、K37ClO3与浓盐酸(HCl)在加热时生成氯气:K37ClO3+6HCl=K37Cl+3Cl2↑+3H2O |
| D、将0.1mol/L盐酸数滴缓缓滴入0.1mol/L25mLNa2CO3溶液中,并不断搅拌:2H++CO32-═CO2↑+H2O |
下列有关中和热和燃烧热的说法中,正确的是( )
| A、进行中和热测定的实验时,不能用环形铁质搅拌棒代替环形玻璃搅拌棒 |
| B、用等体积的0.50mol?L-1盐酸和0.55mol?L-1NaOH溶液进行中和热测定的实验,会使测定结果偏大 |
| C、已知强酸与强碱反应的中和热△H=-57.3kJ?mol-1.所以,1L 1mol?L-1H2SO4与稀NaOH溶液恰好完全反应时,放出57.3kJ的热量 |
| D、已知2C(s)+O2(g)=2CO(g)△H=-220.7kJ?mol-1;所以,C的燃烧热是△H=-220.7kJ?mol-1 |
下列实验装置不适用于物质分离的是( )
A、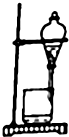 |
B、 |
C、 |
D、 |
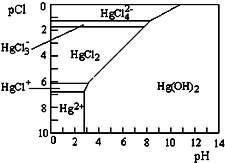 水体中二价汞离子可以与多种阴离子结合成不同的存在形态.水溶液中二价汞主要存在形态与Cl-、OH-的浓度关系如图所示[注:粒子浓度很小时常用负对数表示,如pH=-lgc(H+),pCl=-lgc(Cl-)].
水体中二价汞离子可以与多种阴离子结合成不同的存在形态.水溶液中二价汞主要存在形态与Cl-、OH-的浓度关系如图所示[注:粒子浓度很小时常用负对数表示,如pH=-lgc(H+),pCl=-lgc(Cl-)].