题目内容
6.NA代表阿伏加德罗常数的值.下列叙述正确的是( )| A. | 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2NA | |
| B. | 将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA | |
| C. | 标准状况下,44.8L NO与22.4 L O2反应后的分子数是2NA | |
| D. | 27g铝中加入1mol/L的NaOH溶液,转移电子数是3NA |
分析 A.6.4g混合物中含有6.4gS原子,含有0.2molS原子;
B.氯气和水反应是可逆反应;
C.NO和氧气反应后生成的NO2中存在平衡:2NO2?N2O4;
D.NaOH溶液体积未知;
解答 解:A.6.4g由S2、S4、S8组成的混合物中含有6.4g硫原子,含硫原子的物质的量为:$\frac{6.4g}{32g/mol}$=0.2mol,含有的硫原子数为0.2NA,故A正确;
B.氯气和水反应是可逆反应,在氯水中含氯气分子、HCl和HClO,故溶液中的N(HC1O)+N(Cl-)+N(ClO-)+2N(Cl2)=2NA,故B错误;
C.NO和氧气反应后生成的NO2中存在平衡:2NO2?N2O4,导致分子个数减少,故所得分子个数小于2NA个,故C错误;
D.NaOH溶液体积未知,无法判断铝是否完全反应,无法计算转移电子数,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的计算和判断,题目难度中等,注意明确可逆反应特点,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系是解题关键,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
16.下列各组物质中,相互间一定互为同系物的是( )
| A. | 邻二甲苯和对二甲苯 | B. | C4H8O2和C3H6O2 | ||
| C. | C4H10和C20H42 | D. | C6H5-OH和C6H5-CH2-OH |
17.下列关于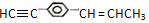 的说法正确的是( )
的说法正确的是( )
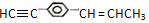 的说法正确的是( )
的说法正确的是( )| A. | 所有碳原子有可能都在同一平面上 | |
| B. | 最多只可能有9个碳原子在同一平面上 | |
| C. | 有7个碳原子可能在同一直线上 | |
| D. | 至少有6个碳原子在同一直线上 |
14.下列实验方案、现象与结论均正确的是( )
| 选项 | 实验方案 | 现象 | 结论 |
| A | 向SiO2固体中加入足量盐酸 | 固体不溶解 | SiO2不溶于任何酸 |
| B | 向Na2CO3溶液中通入足量CO2 | 产生晶体 | 溶解度:NaHCO3>Na2CO3 |
| C | 向75%的酒精中加入小粒钠 | 产生气泡 | 乙醇与钠反应产生H2 |
| D | 向KI 淀粉溶液中通入气体X | 溶液变蓝 | X的氧化性比I2的氧化性强 |
| A. | A | B. | B | C. | C | D. | D |
1. 钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS═Na2Sx,电池结构如图所示.下列说法不正确的是( )
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS═Na2Sx,电池结构如图所示.下列说法不正确的是( )
 钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS═Na2Sx,电池结构如图所示.下列说法不正确的是( )
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS═Na2Sx,电池结构如图所示.下列说法不正确的是( )| A. | 放电时,Na作负极,反应式为Na-e-=Na+ | |
| B. | 钠硫电池在常温下也能正常工作 | |
| C. | 放电时Na+向正极移动 | |
| D. | 当外电路通过0.25mol电子时消耗16g硫,则x=4 |
11.M是中药狼把草的成分之一,具有消炎杀菌作用,其结构如图所示.下列叙述正确的是( )

| A. | M的分子式为C9H10O4 | |
| B. | M与浓溴水既能发生取代反应,又能发生加成反应 | |
| C. | 一定条件下,1 mol M最多能与3molH2发生反应 | |
| D. | M能分别与Na、NaOH、NaHCO3发生反应 |
6.H2是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( )
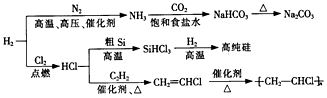

| A. | 使用催化剂可以降低合成氨反应的活化能 | |
| B. | 用澄清石灰水可以检验NaHCO3中是否混有Na2CO3 | |
| C. | 由粗硅制高纯硅的反应类型依次为化合反应、置换反应 | |
| D. | 聚合物 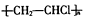 的链节为CH2=CHCl 的链节为CH2=CHCl |