题目内容
13.高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:(1)制备MnSO4溶液:在烧瓶中(装置见图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2,继续反应片刻,过滤.
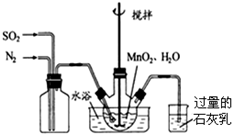
①写出左边集气瓶的作用混合SO2和N2.
②石灰乳的作用是:SO2+Ca(OH)2=CaSO3+H2O(用化学方程式表示)
③写出MnO2和H2SO3反应的离子反应方程式MnO2+H2SO3=Mn2++SO42-+H2O.
④反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有ac(选择选项填空).
a.缓慢通入混合气体 b.快速通入混合气体c.控制适当的温度 d.高温加热
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7.请补充由(1)制得的MnSO4制备高纯MnCO3的操作步骤
【实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH】.
①边搅拌边加入Na2CO3,并控制溶液pH<7.7;
②过滤,水洗2~3次;
③检验SO42-是否被洗涤干净.检验水洗是否合格的方法是取最后一次洗涤的滤液少量于试管,加入用盐酸酸化的BaCl2溶液,若无明显现象,说明水洗合格.
④用少量C2H5OH洗涤,其目的是乙醇容易挥发,便于低温干燥,防止MnCO3受潮被氧化,受热分解;
⑤低于100℃干燥.
分析 (1)①根据实验装置图可知,左边集气瓶的作用是混合SO2和N2;
②石灰乳的作用是吸收尾气二氧化硫,碱和酸性氧化物反应得到对应的盐和水;
③MnO2做氧化剂把亚硫酸氧化为硫酸,自身被还原为Mn2+,据此书写反应的离子方程式;
④为使SO2尽可能转化完全,一定要保证控制反应的温度,在通入SO2和N2比例一定、不改变固液投料的条件下,要求所通气体一定要慢;
(2)制取的原理是碳酸根和锰离子之间反应生成碳酸锰的过程,但要考虑MnCO3难溶于水、乙醇并在潮湿时易被空气氧化,100℃开始分解以及Mn(OH)2开始沉淀时pH=7.7等因素,过程中控制溶液的PH值以及洗涤沉淀所选的溶剂要小心,据此答题.
解答 解:(1)①左边集气瓶可以使通入的SO2和N2混合均匀,故答案为:混合SO2和N2;
②石灰乳的作用是吸收尾气二氧化硫,碱和酸性氧化物反应得到对应的盐和水,反应的化学方程式为:SO2+Ca(OH)2=CaSO3+H2O,
故答案为:SO2+Ca(OH)2=CaSO3+H2O;
③MnO2做氧化剂把亚硫酸氧化为硫酸,自身被还原为Mn2+,反应的离子方程式为:MnO2+H2SO3=Mn2++SO42-+H2O,
故答案为:MnO2+H2SO3=Mn2++SO42-+H2O;
④使SO2尽可能转化完全,应定要保证控制反应的温度,在通入SO2和N2比例一定、不改变固液投料的条件下,要求所通气体一定要慢,
故答案为:ac;
(2)②已知MnCO3难溶于水,所以加入碳酸钠后反应生成碳酸锰,过滤,水洗2~3次,
故答案为:过滤,水洗2~3次;
③检验硫酸根离子是否洗净,可以检验最后一次洗涤液是否含有硫酸根离子,操作方法为:取最后一次洗涤的滤液少量于试管,加入用盐酸酸化的BaCl2溶液,若无明显现象,说明水洗合格,
故答案为:取最后一次洗涤的滤液少量于试管,加入用盐酸酸化的BaCl2溶液,若无明显现象,说明水洗合格;
④已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,乙醇容易挥发,便于低温干燥,防止MnCO3 受潮被氧化,受热分解,
故答案为:乙醇容易挥发,便于低温干燥,防止MnCO3 受潮被氧化,受热分解.
点评 本题主要考查了制备高纯碳酸锰实验方案,题目难度中等,明确工艺流程、正确识图、理解离子反应的本质是解答的关键,试题的综合性强,充分考查了学生的分析能力及化学实验能力.

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:| 实验编号 | HA物质的量浓度 (mol•L-1) | NaOH物质的量浓度 (mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)从第①组情况分析,混合溶液pH=9的原因是A-+H2O?HA+OH-(用离子方程式表示),该组所得混合溶液中由水电离出的c(OH-)=10-5mol•L-1.
(2)第②组情况表明,c>0.2(选填“>”、“<”或“=”),该混合液中离子浓度c(A-) 与c(Na+) 的大小关系是c(A-)=c(Na+).
(3)从第③组实验结果分析,说明此时HA的电离程度>NaA的水解程度(选填“>”、“<”或“=”),该混合溶液中各离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
(4)将一定浓度的NaA溶液稀释100倍时,其pH变化如图 A、B、C曲线中的B(填字母)曲线.
(5)由上述所涉及的溶质组成以下四组等体积溶液:
甲:0.1mol/LNaA
乙:0.1mol/LNaA和0.1mol/LHA
丙:0.1mol/LHA
丁:0.1mol/LNaA和0.1mol/LNaOH
则A-离子浓度由大到小的顺序为乙>丁>甲>丙(填序号).
| A. | Na2CO3是强电解质,BaCO3是弱电解质 | |
| B. | c(H+)=1×10-7mol•L-1的溶液一定呈中性 | |
| C. | 将硫酸铝和氯化铝溶液分别加热蒸干后灼烧,得到的固体都是氧化铝 | |
| D. | 将0.1 mol•L-1醋酸溶液加水稀释时,电离能力增强,但c(H+)变小 |
| 时间/min | 0 | 10 | 20 | 40 | 50 | |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | … | 0.15 |
| A. | T2时CH4的平衡转化率为70.0% | |
| B. | 该反应的△H>0、T1<T2 | |
| C. | 保持其他条件不变,T1时向平衡体系中再充入0.30 mol CH4和0.80 mol H2O(g),平衡向正反应方向移动 | |
| D. | 保持其他条件不变,T1时向平衡体系中再充入0.50 mol CH4和1.20 mol NO2,与原平衡相比,达新平衡时N2的浓度增大、体积分数减小 |
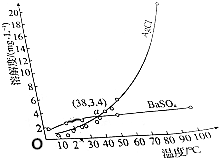
| A. | a点时,AgCl和BaSO4饱和溶液的密度基本相同 | |
| B. | AgCl的溶解是吸热过程 | |
| C. | 室温时,向等体积的饱和AgCl和BaSO4溶液中分别加入足量的浓BaCl2溶液,析出BaSO4沉淀的质量比AgCl多 | |
| D. | 可以用重结晶的方法分离AgCl和BaSO4 |
| A. | 晶体中不存在独立的“分子” | |
| B. | 含有1 mol C的金刚石中,形成的共价键有2 mol | |
| C. | 是自然界中硬度最大的物质 | |
| D. | 化学性质稳定,即使在高温下也不会与氧气发生反应 |
| A. | 用浓硝酸做试剂比较铁和铜的金属活动性 | |
| B. | 使用干燥洁净玻璃棒将氯水滴在干燥pH试纸上,测定氯水的pH | |
| C. | 欲检验Br-的存在,可在溶液中先加入氯水、再加入CCl4,振荡、静置,观察下层溶液显橙红色 | |
| D. | 氢氧化铁胶体在直流电场中,一段时间阴极附近红褐色加深,说明胶体带正电荷 |
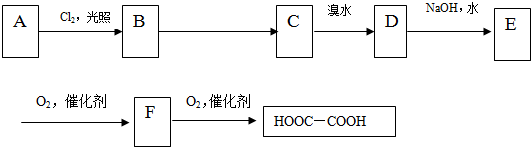
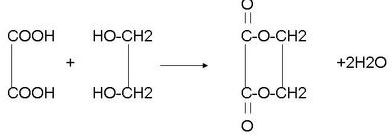 .
. ,含有离子键和非极性共价键的化合物的电子式为
,含有离子键和非极性共价键的化合物的电子式为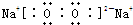 ;含有极性共价键和非极性共价键的化合物的电子式为
;含有极性共价键和非极性共价键的化合物的电子式为 .
. .
.