题目内容
8.三氯化铁是合成草酸铁的重要原料.利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3•5H2O]的实验流程如图1所示: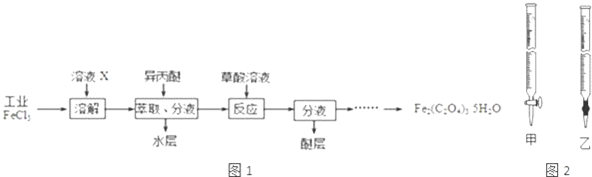
①为抑制FeCl3水解,溶液X为(浓)盐酸.
②上述流程中FeCl3能被异丙醚萃取,其原因是FeCl3在异丙醚中的溶解度大于其在水中的溶解度;检验萃取、分液后所得水层中是否含有Fe3+的方法是取少量溶液,向其中滴加少量KSCN溶液,若溶液变红,则含有Fe3+.
③所得Fe2(C2O4)3•5H2O需用冰水洗涤,其目的是除去杂质、减少草酸铁晶体的溶解损耗.
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于图2所示仪器甲(填“甲”或“乙”)中.下列情况会造成实验测得Fe2(C2O4)3•5H2O含量偏低的是c.
a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数.
分析 利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3•5H2O]的实验流程:工业FeCl3用盐酸溶解,抑制铁离子的水解,FeCl3在异丙醚中的溶解度大于其在水中的溶解度,用异丙醚萃取FeCl3,
①溶解FeCl3用盐酸,抑制水解又不引入杂质;
②萃取是利用溶质在不同溶剂中的溶解度差异分离提取物质的一种方法,能萃取说明FeCl3在异丙醚中的溶解度大于其在水中的溶解度;检验Fe3+用KSCN溶液效果最好;
③洗涤是除去沉淀表面杂质,冰水是减少沉淀溶解损失;故答案为:除去杂质、减少草酸铁晶体的溶解损耗;
④KMnO4标准溶液具有强氧化性,应置于酸式滴定管中;根据高锰酸钾的量计算草酸的含量,
a.没有润洗导致高锰酸钾浓度低消耗体积多;
b.读数高锰酸钾体积多;
c.读数体积偏小,结果偏低.
解答 解:①Fe3+易水解,水解生成H+,水解的离子方程式为Fe3++3H2O?Fe(OH)3+3H+,酸化FeCl3用盐酸酸化,不引入杂质,且抑制铁离子的水解,
故答案为:(浓)盐酸;
②萃取是利用溶质在不同溶剂中的溶解度差异分离提取物质的一种方法,能萃取说明FeCl3在异丙醚中的溶解度大于其在水中的溶解度;检验Fe3+用KSCN溶液效果最好,故答案为:FeCl3在异丙醚中的溶解度大于其在水中的溶解度;取少量溶液,向其中滴加少量KSCN溶液,若溶液变红,则含有Fe3+;
③洗涤是除去沉淀表面杂质,冰水是减少沉淀溶解损失,故答案为:除去杂质、减少草酸铁晶体的溶解损耗;
④KMnO4标准溶液具有强氧化性,能氧化碱式滴定管中的橡胶,应置于酸式滴定管中;
a.没有润洗导致高锰酸钾浓度低消耗体积多,偏高;
b.滴定管滴定前尖嘴部分有气泡,滴定后消失,读数高锰酸钾体积多,偏高;
c.滴定前仰视读数,滴定后俯视读数,读数体积偏小,结果偏低,正确;
故答案为:甲;c.
点评 本题考查盐类水解盐类分析,草酸铁晶体[Fe2(C2O4)3•5H2O]的制备,涉及试验流程问题,根据物质的性质进行分析处理,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 变为原来的10-3倍 | B. | 变为原来的10-2倍 | ||
| C. | 变为原来的10倍 | D. | 不发生变化 |
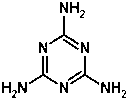
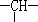 和一个-Cl,则此有机物的结构有( )
和一个-Cl,则此有机物的结构有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
| A. | 该溶液中,H+、Mg2+、NO3-、Cl-可以大量共存 | |
| B. | 该溶液能使红色石蕊试纸变蓝,也能使淀粉碘化钾试纸变蓝 | |
| C. | 该溶液和足量Ba(OH)2溶液反应的离子方程式为:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| D. | 该溶液与过量锌粉反应的离子方程式为:Zn+2Fe3+═2Fe2++Zn2+ |
| A. | NaBr和H2O | B. | Na2O和Na2O2 | C. | D2O和CO2 | D. | NH4Cl和HCl |
| A. | 每一纵行不是主族就是副族 | |
| B. | 短周期原子的次外层电子数都是8个 | |
| C. | 短周期元素是指原子序数为1~20的元素 | |
| D. | 主族元素所在的族序数等于其原子的最外层电子数 |
| A. | 甲烷的二氯代物的同分异构体有两种 | |
| B. | 苯、乙醇和乙酸都能发生取代反应 | |
| C. | 石油分馏的目的是生产乙烯、丙烯、甲烷等化工原料 | |
| D. | 乙酸和乙醇生成乙酸乙酯的反应属于酸碱中和反应 |
 2008年9月11日,全国各地多处发现婴儿因食用三鹿奶粉而出现肾结石的事件.当晚,三鹿集团承认婴幼儿奶粉受到三聚氰胺污染,并宣布召回市面上被污染的产品.三聚氰胺的分子结构如图:有关三聚氰胺的说法正确的是( )
2008年9月11日,全国各地多处发现婴儿因食用三鹿奶粉而出现肾结石的事件.当晚,三鹿集团承认婴幼儿奶粉受到三聚氰胺污染,并宣布召回市面上被污染的产品.三聚氰胺的分子结构如图:有关三聚氰胺的说法正确的是( )| A. | 三聚氰胺属于芳香族化合物,但不属于芳香烃 | |
| B. | 三聚氰胺的分子式为C3N6H6 | |
| C. | 三聚氰胺中的碳原子属于饱和碳原子 | |
| D. | 三聚氰胺分子中的所有原子都在一个平面内 |