题目内容
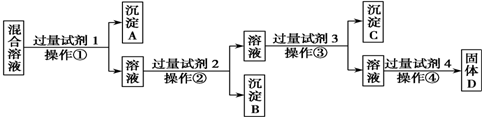
5.现有A、B、C、D、E 5种易溶于水的化合物,已知它们在水溶液中含有的阳离子有K+、Ag+、Al3+、Fe2+、Ba2+;阴离子有Cl-、SO42-、NO3-、CO32-、OH-.(1)不做任何实验,可以确定5种物质中的3种.
(2)分别测定浓度相同5种溶液的pH,测得A、C溶液呈碱性,且A大于C,则C的化学式为K2CO3.
(3)将1 mol•L-1B溶液和1 mol•L-1 D溶液混合无明显现象,则能确定E的化学式为AgNO3.
(4)100 mL 0.1 mol•L-1 D溶液与200 mL 0.1 mol•L-1A溶液混合,生成白色沉淀,充分振荡后最终无沉淀,则D的化学式为AlCl3,该反应的离子方程式为Al3++4OH-=AlO2-+2H2O.
分析 因Ag+只能与NO3-共存,Al3+、Fe2+只能与Cl-、SO42-共存,剩余的K+、Ba2+只能与形成K2CO3、Ba(OH)2,测得A、C溶液呈碱性,且A大于C,则A为Ba(OH)2,C为K2CO3,B与D混合无现象,可知E为AgNO3,D与A反应,为Ba(OH)2与AlCl3反应,以此来解答.
解答 解:因Ag+只能与NO3-共存,Al3+、Fe2+只能与Cl-、SO42-共存,剩余的K+、Ba2+只能与形成K2CO3、Ba(OH)2,测得A、C溶液呈碱性,且A大于C,则A为Ba(OH)2,C为K2CO3,B与D混合无现象,可知E为AgNO3,D与A反应,为Ba(OH)2与AlCl3反应,则D为AlCl3,B为FeSO4,
(1)由上述分析可知,不做实验可确定AgNO3、K2CO3、Ba(OH)2,故答案为:3;
(2)测得A、C溶液呈碱性,且A大于C,因A为强碱,C水解显碱性,C为K2CO3,故答案为:K2CO3;
(3)将1 mol•L-1B溶液和1 mol•L-1 D溶液混合无明显现象,Al3+、Fe2+、Cl-、SO42-之间不反应,可知E为AgNO3,故答案为:E;AgNO3;
(4)100 mL 0.1 mol•L-1 D溶液与200 mL 0.1 mol•L-1A溶液混合,生成白色沉淀,充分振荡后最终无沉淀,则D的化学式为AlCl3,该反应的离子方程式为Al3++4OH-=AlO2-+2H2O,故答案为:AlCl3;Al3++4OH-=AlO2-+2H2O.
点评 本题以离子反应为载体考查无机物的推断,为高频考点,把握离子之间的反应、现象等为解答的关键,侧重分析与推断能力的考查,注意水解及白色沉淀的判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.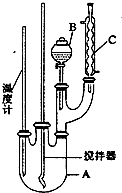 实验室制备硝基苯的反应原理和实验装置如下:
实验室制备硝基苯的反应原理和实验装置如下: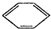 +HO-NO2$→_{50-60℃}^{H_{2}SO_{4}}$
+HO-NO2$→_{50-60℃}^{H_{2}SO_{4}}$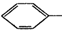 NO2+H2O△H<0
NO2+H2O△H<0
反应中存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯.
有关数据列如下表:
实验步骤如下:①取100mL烧杯,用20mL浓硫酸与18mL浓硝酸配制混和酸,将混合酸小心加入B中;②把18mL(15.84g)苯加入A中;③向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀.在50~60℃下发生反应,直至反应结束;④将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液、水洗涤并分液;⑤分出的产物加入无水CaCl2颗粒,静置片刻,然后倒入蒸馏烧瓶,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g.
回答下列问题:
(1)图中装置C的作用是冷凝回流.
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:不能,容易发生迸溅.
(3)为了使反应在50℃~60℃下进行,常用的方法是水浴加热.反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是溶有浓硝酸分解产生的NO2(或硝酸)等杂质.
(4)在洗涤操作中,第二次水洗的作用是洗去残留的NaOH及生成的盐.
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用水直形冷凝管的原因是以免直形冷凝管通水冷却时导致温差过大而发生炸裂.
(6)本实验所得到的硝基苯产率是72%.
 实验室制备硝基苯的反应原理和实验装置如下:
实验室制备硝基苯的反应原理和实验装置如下: +HO-NO2$→_{50-60℃}^{H_{2}SO_{4}}$
+HO-NO2$→_{50-60℃}^{H_{2}SO_{4}}$ NO2+H2O△H<0
NO2+H2O△H<0反应中存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯.
有关数据列如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二销基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
回答下列问题:
(1)图中装置C的作用是冷凝回流.
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:不能,容易发生迸溅.
(3)为了使反应在50℃~60℃下进行,常用的方法是水浴加热.反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是溶有浓硝酸分解产生的NO2(或硝酸)等杂质.
(4)在洗涤操作中,第二次水洗的作用是洗去残留的NaOH及生成的盐.
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用水直形冷凝管的原因是以免直形冷凝管通水冷却时导致温差过大而发生炸裂.
(6)本实验所得到的硝基苯产率是72%.
13.常温下MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中不正确的是( )
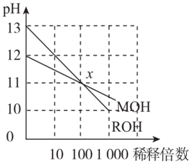

| A. | ROH是一种强碱,MOH是一种弱碱 | |
| B. | 等浓度的MOH与盐酸反应,所得溶液呈中性,则V(MOH)>V(盐酸) | |
| C. | 在x点,c(M+)=c(R+) | |
| D. | 稀释前,c(ROH)=10c(MOH) |
20.某研究性学习小组以元素周期律为课题研究“短周期元素在周期表中的分布”,他们提出元素在周期表中排布的四种方案:
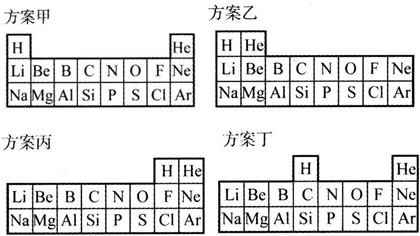
(1)这四种方案都有“合理”的理由,请填写表:
(2)下列化合物中支持方案丙中把H放在第ⅦA族的是D.
A.H2O B.HCl C.NH4Cl D.NaH
(3)下列关系式中支持方案丁中把H放在第ⅣA族的是C.
A.最外层电子数=族序数
B.最高正化合价+|最低负化合价|=8
C.最高正化合价=|最低负化合价|
D.电子层数=周期数
(4)在短周期元素中,原子最外层只有1个或2个电子的元素是D.
A.金属元素
B.稀有气体元素
C.非金属元素
D.无法确定为哪一类元素.

(1)这四种方案都有“合理”的理由,请填写表:
| “合理”的理由 | |
| 方案甲 | |
| 方案乙 | |
| 方案丙 | |
| 方案丁 |
A.H2O B.HCl C.NH4Cl D.NaH
(3)下列关系式中支持方案丁中把H放在第ⅣA族的是C.
A.最外层电子数=族序数
B.最高正化合价+|最低负化合价|=8
C.最高正化合价=|最低负化合价|
D.电子层数=周期数
(4)在短周期元素中,原子最外层只有1个或2个电子的元素是D.
A.金属元素
B.稀有气体元素
C.非金属元素
D.无法确定为哪一类元素.
17.下列关于金属表面氧化膜的说法正确的是( )
| A. | 金属表面的氧化膜都很致密,能对金属起到保护作用 | |
| B. | 金属表面的氧化膜的形成都需要金属暴露在空气中很长时间才会形成 | |
| C. | 金属表面的氧化膜薄层的厚度会随着金属暴露在空气中的时间增长而加厚 | |
| D. | 某些金属表面氧化膜的形成对这些金属的广泛应用起到关键作用 |
14.比较是化学学习中的一种重要方法.下列各组比较中不正确的是( )
| A. | 在相同条件下的溶解度:NaHCO3>Na2CO3 | |
| B. | 热稳定性:HF>HCl>HBr>HI | |
| C. | 氧化性:F2>Cl2>Br2>I2 | |
| D. | 碳酸钠溶液与稀盐酸互滴时,两种操作现象不相同 |
 ;
;