题目内容
8.10g镁铝合金与足量的氢氧化钠溶液反应后,生成气体3.36L(标准状况),则此合金中含镁的质量分数为( )| A. | 35.6% | B. | 27% | C. | 10% | D. | 73% |
分析 发生反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据氢气计算Al的质量,进而计算Mg的质量分数.
解答 解:设合金中Al的质量为m,则:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
54g 3×22.4L
m 3.36L
所以m=$\frac{54g×3.36L}{3×22.4L}$=2.7g
故合金中Mg的质量为10g-2.7g=6.3g
则合金中Mg的质量分数为$\frac{6.3g}{10g}$×100%=63%,
故选:D.
点评 本题考查混合物计算,关键是明确发生的反应,注意方程式计算中左右单位不同时,应左右单位相当,上下单位一致.

练习册系列答案
相关题目
18.足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与3.36L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5mol•L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A. | 60 mL | B. | 90 mL | C. | 120 mL | D. | 45 mL |
16.FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO 和水,当NO2、N2O4、NO的物质的量之比为1:1:1时,实际参加反应的FeS 与HNO3的物质的量之比为( )
| A. | 1:6 | B. | 1:7 | C. | 2:11 | D. | 16:25 |
3.化学与社会、技术、环境、生活密切相关.下列说法正确的是( )
| A. | 碘是人体必需的微量元素,所以要多吃富含高碘酸的食物 | |
| B. | 空气中直径小于或等于2.5?m的颗粒物称为PM2.5 | |
| C. | pH<7的雨水称为酸雨,对环境造成很大的危害 | |
| D. | 甲醛的水溶液可以作为鱿鱼等海鲜的防腐剂 |
20.设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 1mol乙基中含有的电子数为13NA | |
| B. | 标准状况下,22.4L三氯甲烷中共价键数目为4NA | |
| C. | 6.4gCaC2晶体中含有阴阳离子总数为0.3NA | |
| D. | 1mol硫粉与足量的Cu粉共热,转移的电子数为2NA |
17.Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为4Li+2SOCl2═4LiCl+S+SO2,下列说法错误的是( )
| A. | 该电池工作时,正极反应为2SOCl2+4e-═4Cl-+S+SO2 | |
| B. | 锂电极作该电池负极,负极反应为Li-e-═Li+ | |
| C. | 该电池组装时,必须在无水无氧条件下进行 | |
| D. | 该电池工作时,电子通过外电路从正极流向负极 |
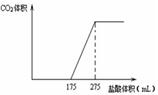 取一定质量NaHCO3和Na2O2的固体混合物放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生气体与所加盐酸体积之间的关系如图所示.试回答下列问题:
取一定质量NaHCO3和Na2O2的固体混合物放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生气体与所加盐酸体积之间的关系如图所示.试回答下列问题: