题目内容
19.设NA为阿伏加德罗常数的数值,下列说法中正确的是( )| A. | 标准状况下,22.4L Cl2完全溶于水时,转移电子数为NA | |
| B. | 常温下,0.1mol/L NH4NO3溶液中NO3-的数目为0.1NA | |
| C. | 室温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| D. | 常温下,23g NO2和N2O4的混合气体中含有NA个氧原子 |
分析 A、氯气和水的反应为可逆反应;
B、溶液体积不明确;
C、室温下,铁在浓硫酸中会钝化;
D、NO2和N2O4的最简式均为NO2.
解答 解:A、氯气和水的反应为可逆反应,不能进行彻底,故转移的电子的个数小于NA个,故A错误;
B、溶液体积不明确,故溶液中的硝酸根的个数无法计算,故B错误;
C、室温下,铁在浓硫酸中会钝化,进行程度很小,故生成的二氧化硫分子个数小于NA个,故C错误;
D、NO2和N2O4的最简式均为NO2,故23g混合物中含有的NO2的物质的量为n=$\frac{23g}{46g/mol}$=0.5mol,故含1mol氧原子即NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
7.PCl3和PCl5都是重要的化工原料.将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下发生反应:PCl3(g)+Cl2(g)?PCl5(g),并于10min时达到平衡.有关数据如下:
下列判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol•L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol•L-1) | c1 | c2 | 0.4 |
| A. | 10 min内,v(Cl2)=0.04 mol•L-1•min-1 | |
| B. | 当容器中Cl2为1.2 mol时,反应达到平衡 | |
| C. | 升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3$\frac{△n({T}_{1})}{△n({T}_{2})}$<1 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件再达平衡时,c(PCl5)<0.2 mol•L-1 |
7.下列叙述中,正确的是( )
| A. | 氯化铝溶液中加入过量氨水反应的实质:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| B. | 在加入铝粉能放出氢气的溶液中,K+、NO3-、CO32-、Cl-一定能够大量共存 | |
| C. | 铁和稀HNO3反应后,溶液pH=2:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O | |
| D. | 1 L0.1 mol•L-1FeCl3溶液和足量的Zn充分反应,生成11.2 g Fe |
4.下列改变一定能说明化学平衡发生移动的是( )
| A. | 反应混合物中各物质的浓度的改变 | B. | 反应物转化率的改变 | ||
| C. | 正逆反应速率的改变 | D. | 反应容器中压强的改变 |
9.验证某有机物是由C、H、O三种元素组成的烃的衍生物,应完成的实验内容是( )
| A. | 测定它的碳、氢元素的质量比 | |
| B. | 只要证明它完全燃烧后产物有H2O和CO2 | |
| C. | 测定其产物中H2O和CO2的比值 | |
| D. | 测定该试样质量及试样完全燃烧后产物的质量 |
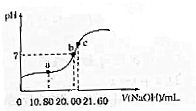 草酸(H2C2O4,二元酸弱)与草酸盐在实验和工业生产中都起着重要的作用.
草酸(H2C2O4,二元酸弱)与草酸盐在实验和工业生产中都起着重要的作用. 如图为实验室某浓盐酸试剂瓶标签上的数据,请根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的数据,请根据有关数据回答下列问题: