题目内容
某元素X的气态氢化物的化学式为XH4,则X的最高价氧化物的水化物的化学式为( )
| A、H3XO4 |
| B、H2XO4 |
| C、H2XO3 |
| D、HXO3 |
考点:根据化合价正确书写化学式(分子式)
专题:物质的组成专题
分析:根据元素X的气态氢化物的化学式确定元素X的最低负价,而元素的最高正价+|最低负价|=8,进而求得X元素最高正价,结合选项各化学式中X元素的化合价,据此判断.
解答:
解:元素X的气态氢化物的化学式为XH4,所以X的最低负价为-4价,所以元素R的最高正价为+4价,X的最高价氧化物的水化物的化学式为H2XO3,故选C.
点评:本题考查学生元素周期律的应用知识,难度不大,注意掌握元素的最高正价+|最低负价|=8,根据化学式计算元素化合价.

练习册系列答案
相关题目
下列化学用语表达正确的是( )
| A、一氯乙烷的结构式CH3Cl |
| B、丁烷的结构简式CH3(CH2)2CH3 |
C、四氯化碳的电子式 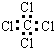 |
D、C2H4分子比例模型: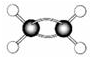 |
用图示装置(试剂任选)能完成下列实验的是( )
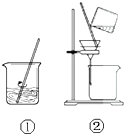

| A、从粗盐中获得NaCl晶体 |
| B、除去附着在铁屑表面的铝 |
| C、从含苯酚的废水中回收苯酚 |
| D、除去Fe(OH)3胶体中的FeCl3 |
长周期元素周期表共有18个竖行,从左到右排为1~18列,即碱金属是第一列,稀有气体是第18列.按这种规定,下面说法正确的是( )
| A、第13列元素中没有非金属 |
| B、第15列元素的原子最外层的排布是ns2np3 |
| C、最外层电子数为ns2的元素在第2列 |
| D、10、11列为ds区的元素 |
下列有关化学平衡常数K的叙述正确的是( )
| A、与反应温度有关 |
| B、与反应物性质有关 |
| C、与反应物浓度有关 |
| D、与反应物接触面积有关 |
粗盐提纯实验用到的试剂中,不是为了除去原溶液中杂质离子的是( )
| A、盐酸 | B、烧碱溶液 |
| C、纯碱溶液 | D、氯化钡溶液 |
不能说明X的非金属性比Y强的是( )
| A、X原子的最外层电子数比Y原子的最外层电子数多 |
| B、X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 |
| C、与H2化合时X单质比Y单质容易 |
| D、X单质可以把Y从其氢化物中置换出来 |
下列溶液中微粒的物质的量浓度关系正确的是( )
| A、氯水中:c(Cl2)=2c(ClO-)+2c(Cl-)+2c(HClO) |
| B、Na2CO3溶液:c(OH-)-c(H+)═c(HCO3-)+2 c(H2CO3) |
| C、等浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)═c(HCO3-)+c(H2CO3) |
| D、室温下,向0.01 mol/L NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
如图是周期表中短周期的一部分,A、B的原子序数之和等于C原子的原子序数.下列叙述正确的是( )


| A、C的氧化物对应的水化物一定为强酸,且只有氧化性 |
| B、三种元素对应的氢化物中B的氢化物稳定性最好 |
| C、原子半径大小关系为:B>A |
| D、C的单质常温下为无色无味的气体 |