题目内容
常温时,向pH=12的Ba(OH)2溶液中加入等体积的下列溶液后,滴入酚酞试液出现红色,该溶液应该是( )
| A、pH=2的硫酸溶液 |
| B、pH=2的醋酸溶液 |
| C、0.05mol/L盐酸溶液 |
| D、0.05mol/LNa2SO4溶液 |
考点:酸碱混合时的定性判断及有关ph的计算
专题:
分析:A、向pH=12的Ba(OH)2溶液中加入pH=2的硫酸溶液,等体积混合氢离子氢氧根离子恰好反应;
B、向pH=12的Ba(OH)2溶液中加入等体积pH=2的醋酸溶液,醋酸平衡状态氢离子浓度和氢氧化钡溶液中氢氧根离子浓度相同,恰好反应,醋酸是弱酸又电离出氢离子,溶液呈酸性;
C、向pH=12的Ba(OH)2溶液c(OH-)=0.01mol/L,加入等体积0.05mol/L盐酸溶液,盐酸过量,溶液呈酸性;
D、向pH=12的Ba(OH)2溶液c(OH-)=0.01mol/L,Ba(OH)2溶液浓度0.005mol/L,溶液中加入等体积0.05mol/LNa2SO4溶液,生成硫酸钡和氢氧化钠溶液,溶液呈碱性;
B、向pH=12的Ba(OH)2溶液中加入等体积pH=2的醋酸溶液,醋酸平衡状态氢离子浓度和氢氧化钡溶液中氢氧根离子浓度相同,恰好反应,醋酸是弱酸又电离出氢离子,溶液呈酸性;
C、向pH=12的Ba(OH)2溶液c(OH-)=0.01mol/L,加入等体积0.05mol/L盐酸溶液,盐酸过量,溶液呈酸性;
D、向pH=12的Ba(OH)2溶液c(OH-)=0.01mol/L,Ba(OH)2溶液浓度0.005mol/L,溶液中加入等体积0.05mol/LNa2SO4溶液,生成硫酸钡和氢氧化钠溶液,溶液呈碱性;
解答:
解:常温下,酚酞溶液PH变色范围8--10
A、向pH=12的Ba(OH)2溶液中加入pH=2的硫酸溶液,等体积混合氢离子和氢氧根离子恰好反应,溶液呈中性,故A错误;
B、向pH=12的Ba(OH)2溶液中加入等体积pH=2的醋酸溶液,醋酸平衡状态氢离子浓度和氢氧化钡溶液中氢氧根离子浓度相同,恰好反应,醋酸是弱酸又电离出氢离子,溶液呈酸性,滴入酚酞试液不出现红色,故B错误;
C、向pH=12的Ba(OH)2溶液c(OH-)=0.01mol/L,加入等体积0.05mol/L盐酸溶液,盐酸过量,溶液呈酸性,滴入酚酞试液不出现红色,故C错误;
D、向pH=12的Ba(OH)2溶液c(OH-)=0.01mol/L,Ba(OH)2溶液浓度0.005mol/L,溶液中加入等体积0.05mol/LNa2SO4溶液,生成硫酸钡和氢氧化钠溶液,溶液呈碱性,滴入酚酞试液出现红色,故D正确;
故选D.
A、向pH=12的Ba(OH)2溶液中加入pH=2的硫酸溶液,等体积混合氢离子和氢氧根离子恰好反应,溶液呈中性,故A错误;
B、向pH=12的Ba(OH)2溶液中加入等体积pH=2的醋酸溶液,醋酸平衡状态氢离子浓度和氢氧化钡溶液中氢氧根离子浓度相同,恰好反应,醋酸是弱酸又电离出氢离子,溶液呈酸性,滴入酚酞试液不出现红色,故B错误;
C、向pH=12的Ba(OH)2溶液c(OH-)=0.01mol/L,加入等体积0.05mol/L盐酸溶液,盐酸过量,溶液呈酸性,滴入酚酞试液不出现红色,故C错误;
D、向pH=12的Ba(OH)2溶液c(OH-)=0.01mol/L,Ba(OH)2溶液浓度0.005mol/L,溶液中加入等体积0.05mol/LNa2SO4溶液,生成硫酸钡和氢氧化钠溶液,溶液呈碱性,滴入酚酞试液出现红色,故D正确;
故选D.
点评:本题考查了算教案中和反应后溶液酸碱性的分析判断和计算,掌握基础是解题关键,题目难度中等.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
当用酸滴定碱时,下列操作使滴定结果(碱的浓度)偏高的是( )
| A、酸式滴定管滴至终点,俯视读数 |
| B、碱液移入锥形瓶后,加入10mL蒸馏水 |
| C、酸式滴定管注入酸溶液后,尖嘴无气泡时开始滴定,滴定后有气泡 |
| D、酸式滴定管用蒸馏水洗涤后,未用标准液润洗 |
水的电离平衡曲线如图所示,下列说法不正确的是( )
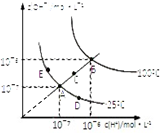

| A、图中五点KW间的关系:B>C>A=D=E |
| B、若从A点到D点,可采用:温度不变时在水中加入少量酸 |
| C、在B点对应的温度下,将pH=2的硝酸与pH=10的Ba(OH)2(aq)等体积混合后,溶液显中性 |
| D、若从A点到C点,可采用:温度不变时在水中加入适量的NH4Cl固体 |
 利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,其它条件相同的情况下,使用不同催化剂(Ⅰ,Ⅱ,Ⅲ),CH4的产量随光照时间的变化如图所示.
利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,其它条件相同的情况下,使用不同催化剂(Ⅰ,Ⅱ,Ⅲ),CH4的产量随光照时间的变化如图所示.
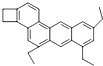 (Ⅰ)乙苯的结构简式可以表示为
(Ⅰ)乙苯的结构简式可以表示为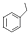 ,下图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”.
,下图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”.