题目内容
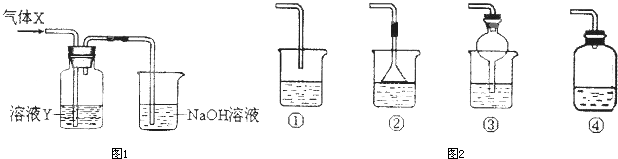
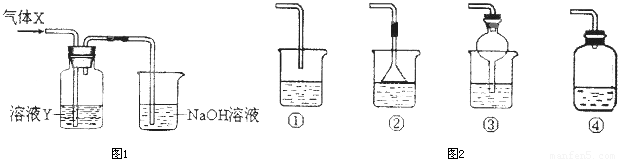
某化学实验小组同学用如图所示装置进行系列实验,以探究气体的性质(部分仪器已略去).请回答: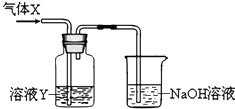
(1)若气体X为氯气,溶液Y为含有少量KSCN的FeCl2溶液,则可观察到溶液Y中的实验现象是
(2)若溶液Y为品红溶液,气体X通过后,溶液褪色,取少量褪色后的溶液加热后恢复为红色,则气体X可能是

(1)若气体X为氯气,溶液Y为含有少量KSCN的FeCl2溶液,则可观察到溶液Y中的实验现象是
溶液变为红色
溶液变为红色
反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,Fe 3++3SCN-=Fe(SCN)3
2Fe2++Cl2=2Fe3++2Cl-,Fe 3++3SCN-=Fe(SCN)3
;NaOH溶液中发生反应的离子方程式是Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
(2)若溶液Y为品红溶液,气体X通过后,溶液褪色,取少量褪色后的溶液加热后恢复为红色,则气体X可能是
SO2
SO2
(填化学式).分析:(1)氯气有强氧化性,能把亚铁离子氧化生成铁离子,铁离子能和硫氰根离子反应生成红色的络合物,氯气能和氢氧化钠反应生成氯化钠和次氯酸钠、水;
(2)二氧化硫能使品红溶液褪色,且褪色后的溶液加热能恢复原色.
(2)二氧化硫能使品红溶液褪色,且褪色后的溶液加热能恢复原色.
解答:解:(1)氯气有强氧化性,能把亚铁离子氧化生成铁离子,离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,铁离子能和硫氰根离子反应生成红色的络合物,所以溶液呈红色,离子方程式为:Fe 3++3SCN-=Fe(SCN)3,氯气能和氢氧化钠反应生成氯化钠和次氯酸钠、水,离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:溶液变为红色,2Fe2++Cl2=2Fe3++2Cl-,Fe 3++3SCN-=Fe(SCN)3;Cl2+2OH-=Cl-+ClO-+H2O;
(2)二氧化硫能使品红溶液褪色,且褪色后的溶液加热能恢复原色,所以该气体可能是SO2,故答案为:SO2.
故答案为:溶液变为红色,2Fe2++Cl2=2Fe3++2Cl-,Fe 3++3SCN-=Fe(SCN)3;Cl2+2OH-=Cl-+ClO-+H2O;
(2)二氧化硫能使品红溶液褪色,且褪色后的溶液加热能恢复原色,所以该气体可能是SO2,故答案为:SO2.
点评:本题以性质实验方案设计为载体考查了氯气和二氧化硫的性质,铁离子的检验是高考的热点,应掌握该知识点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目