题目内容
3.已知:P4(白磷,s)+5O2(g)═P4O10(s)△H=-2983.2kJ/mol,P(红磷,s)+$\frac{5}{4}$O2(g)═$\frac{1}{4}$P4O10(s)△H=-738.5kJ/mol.
试写出白磷转化为红磷的热化学方程式P4(白磷,s)=4 P(红磷,s)△H=-29.2 kJ/mol;
相同状况下,能量较低的是红磷,白磷的稳定性低于红磷(填“高”或“低”).
分析 P4(s,白磷)+5O2(g)=P4O10(s)△H1=-2983.2kJ/mol…①
P(s,红磷)+$\frac{5}{4}$O2(g)=$\frac{1}{4}$P4O10(s)△H2=-738.5kJ/mol…②
①-②×4可得:P4(s,白磷)=4P(s,红磷),根据盖斯定律写出白磷转化为红磷的焓变,书写热化学方程式,根据物质的总能量与反应热的关系判断,能量越高物质越稳定.
解答 解:P4(s,白磷)+5O2(g)=P4O10(s)△H1=-2983.2kJ/mol…①
P(s,红磷)+$\frac{5}{4}$O2(g)=$\frac{1}{4}$P4O10(s)△H2=-738.5kJ/mol…②
根据盖斯定律:①-②×4可得:P4(s,白磷)=4P(s,红磷)△H=(-2983.2kJ/mol)-(-738.5kJ)×4=-29.2kJ/mol,
说明白磷转化为红磷是放热反应,相同的状况下,能量比白磷低,而能量越低,物质越稳定,故白磷稳定性低于红磷,
故答案为:P4(白磷,s)=4 P(红磷,s)△H=-29.2 kJ/mol;红磷;低.
点评 本题考查了热化学方程式书写、盖斯定律的应用以及反应热和物质的能量之间的关系,题目难度中等.

练习册系列答案
相关题目
14.下列操作方法或实验装置正确的是( )
| A. | 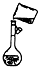 向容量瓶中转移液体 | B. |  向试管内滴加液体 | ||
| C. | 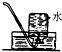 氨气的收集 | D. | 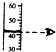 量取液体时读数 |
11.中学阶段介绍的应用电解法制备的物质主要有三种:一是金属铝的冶炼、二是氯碱工业、三是金属钠的制备.下列关于这三个工业生产的描述中正确的是( )
| A. | 电解法制铝时,一般用熔融态的氧化铝进行电解,但也可用其相应的盐,如熔融态的AlCl3 | |
| B. | 电解法生产铝时,需对铝土矿进行提纯,在提纯过程中应用了氧化铝或氢氧化铝的两性 | |
| C. | 在氯碱工业中,电解池中的阴极产生的是H2,NaOH在阳极附近产生 | |
| D. | 氯碱工业和金属钠的冶炼都用到了NaCl,在电解时它们的阴极都是Cl-失电子 |
18.下列实验操作中叙述正确的是( )
| A. | 萃取操作必须在分液漏斗中进行 | |
| B. | 振荡试管中液体时,手拿住试管,用手腕甩动 | |
| C. | 用剩的药品应收集起来放回原试剂瓶中 | |
| D. | 称量物质时先取小砝码,再依次取较大的砝码 |
8.某种盐与浓硫酸及铜共热,有红棕色气体生成;该盐与烧碱混合共热,有能使湿润的红色石蕊试纸变蓝的无色气体生成.有关该盐的叙述不正确的是( )
| A. | 该盐的名称为硝酸铵 | B. | 该盐的水溶液pH<7 | ||
| C. | 该盐的化学式为NH4HCO3 | D. | 该盐可做氮肥,不宜与草木灰混用 |
15.下列叙述中正确的是( )
| A. | 摩尔是物质的质量的单位 | |
| B. | 碳的摩尔质量为12g | |
| C. | 阿伏加德罗常数约为6.02×1023mol-1 | |
| D. | 一个碳原子的质量为12g |
12.离子方程式2Ca2++3HCO3-+3OH-→2CaCO3↓+CO32-+3H2O可以表示( )
| A. | Ca(HCO3)2与NaOH溶液反应 | B. | Mg(HCO3)2与NaOH溶液反应 | ||
| C. | Ca(HCO3)2与澄清石灰水反应 | D. | NH4HCO3与澄清石灰水反应 |
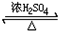 CH3COOC2H5+H2O,属于酯化(取代)反应.
CH3COOC2H5+H2O,属于酯化(取代)反应.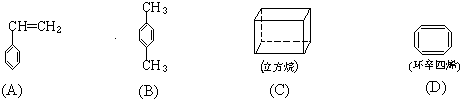 )是一种重要的化工原料.将苯乙烯通入到溴水中,反应的化学方程式为:C6H5-CH=CH2+Br2→C6H5-CHBr-CH2Br.
)是一种重要的化工原料.将苯乙烯通入到溴水中,反应的化学方程式为:C6H5-CH=CH2+Br2→C6H5-CHBr-CH2Br. .
.