题目内容
下列反应属于吸热反应的是( )
| A、盐酸和氢氧化钠溶液之间的中和反应 | ||||
B、CO2+C
| ||||
C、金属镁燃烧:2Mg+O2
| ||||
| D、生石灰溶于水:CaO+H2O=Ca(OH)2 |
考点:吸热反应和放热反应
专题:化学反应中的能量变化
分析:根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应等,
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),氢氧化钡与氯化铵的反应,少数分解置换以及某些复分解(如铵盐和强碱)等.
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),氢氧化钡与氯化铵的反应,少数分解置换以及某些复分解(如铵盐和强碱)等.
解答:
解:A.盐酸与氢氧化钠溶液的中和反应,是放热反应,故A错误;
B.碳与二氧化碳的反应是吸热反应,故B正确;
C.金属镁燃烧属于放热反应,故C错误;
D.生石灰溶于水属于放热反应,故D错误.
故选B.
B.碳与二氧化碳的反应是吸热反应,故B正确;
C.金属镁燃烧属于放热反应,故C错误;
D.生石灰溶于水属于放热反应,故D错误.
故选B.
点评:本题考查吸热反应和放热反应,难度不大,掌握中学化学中常见的吸热或放热的反应是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
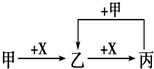 已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合如图.则甲和X(要求甲和X能互换)不可能是[提示:Al3++3AlO2-+6H2O=4Al(OH)3↓]( )
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合如图.则甲和X(要求甲和X能互换)不可能是[提示:Al3++3AlO2-+6H2O=4Al(OH)3↓]( )| A、C和O2 |
| B、SO2和NaOH溶液 |
| C、Cl2和Fe |
| D、AlCl3溶液和NaOH溶液 |
25℃时,NH4Cl和NH3?H2O混合溶液的pH为7,则该溶液呈( )
| A、酸性 | B、碱性 |
| C、中性 | D、无法确定 |
关于下列图示的说法中正确的是( )
A、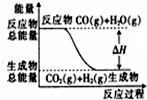 表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”中的△H>0 |
B、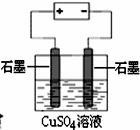 为电解硫酸铜溶液的装置,电解前后溶液的pH几乎不变 |
C、 实验装置可完成比较乙酸、碳酸、硅酸酸性强弱的实验 |
D、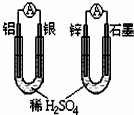 两个装置通过的电量相等时,消耗负极材料的物质的量也相同 |
下列说法正确的是( )
| A、增大压强,使活化分子数目增加,化学反应速率一定增大 |
| B、活化分子间所发生的分子间碰撞均为有效碰撞 |
| C、升高温度,使活化分子百分数增加,化学反应速率一定增大 |
| D、加入反应物,使活化分子百分数增加,化学反应速率一定增大 |
在3S+6KOH=2K2S+K2SO3+3H2O这个反应中,被氧化与被还原的S原子个数比( )
| A、1:2 | B、2:1 |
| C、1:1 | D、3:1 |
阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是( )
| A、1molN2所含分子数约为6.02×1023 |
| B、58.5g NaCl所含离子数约为6.02×1023 |
| C、标准状况下,22.4L H2所含原子数约为6.02×1023 |
| D、常温常压下,分子总数约为6.02×1023的SO2的质量是64 |